Naukowiec ujawnia fuszerkę w badaniach nad szczepionką firmy Pfizer
Ujawnienie złych praktyk stosowanych przez firmę badawczą pomagającą Pfizerowi w przeprowadzeniu kluczowego badania nad szczepionką Covid-19 rodzi pytania o integralność danych i nadzór regulacyjny.

Jesienią 2020 roku prezes i dyrektor generalny firmy Pfizer, Albert Bourla, wystosował list otwarty do miliardów ludzi na całym świecie, którzy pokładali nadzieję w bezpiecznej i skutecznej szczepionce przeciwko Covid-19, która miałaby położyć kres pandemii. „Jak już wcześniej wspomniałem, działamy z prędkością nauki” – napisał Bourla, wyjaśniając opinii publicznej, kiedy może się ona spodziewać dopuszczenia szczepionki firmy Pfizer do obrotu w Stanach Zjednoczonych[1].
Jednak dla naukowców, którzy testowali szczepionkę firmy Pfizer w kilku ośrodkach w Teksasie jesienią tamtego roku, taka szybkość działania mogła odbić się kosztem integralności danych i bezpieczeństwa pacjentów. Dyrektor regionalny, która była zatrudniona w organizacji badawczej Ventavia Research Group, powiedziała czasopismu British Medical Journal [BMJ], że firma fałszowała dane, odślepiała pacjentów, zatrudniała nieodpowiednio przeszkolonych szczepionkarzy i nie nadążała z monitorowaniem zdarzeń niepożądanych zgłaszanych w kluczowym badaniu III fazy przeprowadzonym przez podwykonawcę dla firmy Pfizer. Pracownicy przeprowadzający kontrole jakości byli przytłoczeni ilością problemów, które znajdowali. Po wielokrotnym powiadamianiu firmy Ventavia o tych problemach, dyrektorka regionalna, Brook Jackson, wysłała skargę pocztą elektroniczną do Amerykańskiej Agencji Żywności i Leków (FDA). Ventavia zwolniła ją jeszcze tego samego dnia. Jackson dostarczyła The BMJ dziesiątki wewnętrznych dokumentów firmowych, zdjęć, nagrań audio i e-maili.
Badania kliniczne szczepionek na Covid-19 pokazują, że protokoły opracowane są tak, żeby zakończyły się sukcesem. – prof. William A. Haseltine
O stronniczości badań i publikacji finansowanych przez przemysł farmaceutyczny
Czy na pewno szczepionki to najlepiej przebadane produkty firm farmaceutycznych? Sprawdźmy.
Słabe zarządzanie laboratorium
Na swojej stronie internetowej firma Ventavia nazywa siebie największą prywatną firmą zajmującą się badaniami klinicznymi w Teksasie i wymienia wiele nagród, które zdobyła za swoją pracę kontraktową[2]. Jednakże Brook Jackson powiedziała czasopismu BMJ, że podczas dwóch tygodni, kiedy była zatrudniona w Ventavii we wrześniu 2020 roku, wielokrotnie informowała swoich przełożonych o złym zarządzaniu laboratorium, obawach dotyczących bezpieczeństwa pacjentów i problemach z integralnością danych. Brook Jackson była wyszkolonym audytorem badań klinicznych, która wcześniej zajmowała stanowisko dyrektora ds. operacji i przyszła do firmy Ventavia z ponad 15-letnim doświadczeniem w koordynacji i zarządzaniu badaniami klinicznymi. Rozgoryczona tym, że Ventavia nie radzi sobie z problemami, Brook Jackson udokumentowała kilka spraw późno w nocy, robiąc zdjęcia telefonem komórkowym. Jedno ze zdjęć, dostarczone do BMJ, pokazywało igły wyrzucone w plastikowej torbie na biologiczne odpady niebezpieczne zamiast do pojemnika na ostre narzędzia. Inne pokazywało materiały opakowaniowe szczepionek z wypisanymi na nich numerami identyfikacyjnymi uczestników badania pozostawione na otwartej przestrzeni, potencjalnie odślepiając uczestników. Kierownictwo Ventavii później przesłuchało ją za zrobienie tych zdjęć.
Wczesne i nieumyślne odślepianie mogło mieć miejsce na znacznie szerszą skalę. Zgodnie z projektem badania, nieoślepiony personel był odpowiedzialny za przygotowanie i podawanie eksperymentalnego preparatu (szczepionki firmy Pfizer lub placebo). Miało to służyć zachowaniu zaślepienia uczestników badania i wszystkich innych pracowników ośrodka, w tym głównego badacza. Jednak w Ventavii Brook Jackson powiedziała, że wydruki potwierdzające przypisanie leku były pozostawiane w kartach uczestników, dostępne dla zaślepionego personelu. W ramach działań naprawczych podjętych we wrześniu, dwa miesiące po rozpoczęciu rekrutacji do badania i przy około 1000 już zapisanych uczestnikach, listy kontrolne zapewnienia jakości zostały zaktualizowane o instrukcje dla personelu, aby usunąć przypisania leków z kart.
W nagraniu ze spotkania pod koniec września 2020 roku pomiędzy Brook Jackson i dwoma dyrektorami można usłyszeć, jak członek zarządu Ventavii wyjaśnia, że firma nie była w stanie określić ilościowo rodzajów i liczby błędów, które znajdowała podczas sprawdzania dokumentacji związanej z badaniami pod kątem kontroli jakości. „Według mnie, każdego dnia pojawia się coś nowego” – mówi członek zarządu Ventavii. „Wiemy, że jest to znaczące”.
Ventavia nie nadążała ogarniać zapytań dotyczących danych, wskazuje na to wiadomość e-mail wysłana od pracownika firmy ICON, kontraktową organizację badawczą, z którą Pfizer współpracował przy badaniu. [Oferują usługi konsultingowe, dotyczące rozwoju klinicznego i komercjalizacji produktów]. ICON przypomniał Ventavii w wiadomości e-mail z września 2020 r: „Oczekiwaniem dla tego badania jest to, że wszystkie zapytania są adresowane w ciągu 24 godzin„. Następnie ICON zaznaczył na żółto ponad 100 zaległych zapytań starszych niż trzy dni. Przykłady obejmowały dwie osoby, dla których „Podmiot zgłosił się z ciężkimi objawami/reakcjami … Zgodnie z protokołem, należy skontaktować się z uczestnikami doświadczającymi reakcji miejscowych stopnia 3. Proszę potwierdzić, czy doszło do NIEPLANOWANEGO KONTAKTU i odpowiednio zaktualizować odpowiedni formularz.” Zgodnie z protokołem badania kontakt telefoniczny powinien był nastąpić „w celu ustalenia dalszych szczegółów i określenia, czy wizyta w miejscu badania jest klinicznie wskazana.”
Obawy związane z inspekcją FDA
Dokumenty pokazują, że problemy trwały już od tygodni. Na liście „rzeczy do zrobienia”, która krążyła wśród kierownictwa Ventavii na początku sierpnia 2020, krótko po rozpoczęciu badań klinicznych i przed zatrudnieniem Brook Jackson, dyrektor Ventavii zidentyfikował trzech pracowników, z którymi należy „Przejrzeć sprawę e-dziennika/fałszowania danych, itp.”. Jeden z nich został „ustnie upomniany za zmianę danych i nie odnotowywanie ostatnich wpisów”, wskazuje notatka.
W kilku punktach podczas spotkania pod koniec września Brook Jackson i dyrektorzy Ventavii dyskutowali o możliwości pojawienia się FDA w celu przeprowadzenia inspekcji (ramka 1). „Dostaniemy przynajmniej jakiś list informacyjny, kiedy FDA tu dotrze… rozumiesz.” – stwierdził jeden z dyrektorów.
Odporność i bezkarność: korupcja w relacjach Państwo-Farmacja – dr Paddy Rawlinson
Ramka 1
Historia niedbałego nadzoru
Jeśli chodzi o FDA i badania kliniczne, Elizabeth Woeckner, prezes Citizens for Responsible Care and Research Incorporated (CIRCARE)[3], twierdzi, że możliwości nadzorcze agencji są poważnie niedofinansowane. Jeśli FDA otrzymuje skargę na badania kliniczne, mówi, że agencja rzadko ma personel dostępny, aby pojawić się i przeprowadzić inspekcję. A czasami nadzór pojawia się zbyt późno.
W jednym z przykładów, CIRCARE i amerykańska organizacja rzeczników konsumentów Public Citizen, wraz z dziesiątkami ekspertów zdrowia publicznego, złożyli szczegółową skargę w lipcu 2018 r. do FDA na badanie kliniczne, które nie spełniało przepisów dotyczących ochrony uczestników ludzkich.[4] Dziewięć miesięcy później, w kwietniu 2019 r., śledczy FDA przeprowadził inspekcję w ośrodku klinicznym. W maju tego roku FDA wysłała placówce prowadzącej badania kliniczne list ostrzegawczy, który uzasadniał wiele twierdzeń zawartych w skargach. Stwierdzono w nim, że “Wygląda na to, że nie stosowali się Państwo do obowiązujących wymogów ustawowych i przepisów FDA regulujących prowadzenie badań klinicznych i ochronę osób biorących w nich udział[5].”
„Istnieje całkowity brak nadzoru nad kontraktowymi organizacjami badawczymi i niezależnymi ośrodkami badań klinicznych” – mówi Jill Fisher, profesor medycyny społecznej na University of North Carolina School of Medicine i autorka książki Medical Research for Hire: The Political Economy of Pharmaceutical Clinical Trials [Badania medyczne do wynajęcia: Ekonomia polityczna farmaceutycznych badań klinicznych]”.
Ventavia i FDA
Była pracowniczka firmy Ventavia powiedziała BMJ, że ludzie w firmie byli zdenerwowani i spodziewali się federalnego audytu swoich badań nad szczepionką Pfizera.
„Ludzie pracujący przy badaniach klinicznych są przerażeni audytami FDA” – powiedziała Jill Fisher w rozmowie z BMJ, ale dodała, że agencja rzadko zajmuje się czymś innym niż sprawdzaniem dokumentacji, zazwyczaj miesiące po zakończeniu badania. „Nie wiem, dlaczego tak się ich boją,” powiedziała. Jednakże powiedziała, że była zaskoczona, że agencja nie przeprowadziła inspekcji Ventavii po tym jak pracownik złożył skargę. „Można by pomyśleć, że jeśli pojawia się konkretna i wiarygodna skarga, to będą musieli to zbadać,” powiedziała Jill Fisher.
W 2007 roku Biuro Inspektora Generalnego Departamentu Zdrowia i Usług Społecznych [HHS] opublikowało raport na temat nadzoru FDA nad badaniami klinicznymi przeprowadzonymi w latach 2000-2005. Raport wykazał, że FDA skontrolowała jedynie 1% ośrodków zajmujących się badaniami klinicznymi[6]. Inspekcje przeprowadzone przez oddział FDA zajmujący się szczepionkami i produktami biologicznymi w ostatnich latach malały, a w roku fiskalnym 2020 przeprowadzono ich zaledwie 50[7].
Następnego ranka, 25 września 2020 r., Brook Jackson zadzwoniła do FDA, aby ostrzec o niewłaściwych praktykach w badaniach klinicznych firmy Pfizer w Ventavii. Następnie zgłosiła swoje obawy w wiadomości e-mail do agencji. Po południu firma Ventavia ją zwolniła – została uznana za „nie pasującego pracownika”, zgodnie z jej listem separacyjnym.
Brook Jackson powiedziała czasopismu BMJ, że to był pierwszy raz kiedy została zwolniona w jej 20-letniej karierze w badaniach.
Zgłoszone obawy
W swoim mailu z 25 września do FDA Brook Jackson napisała, że firma Ventavia zapisała ponad 1000 uczestników w trzech miejscach. Pełne badanie kliniczne (zarejestrowane pod nr NCT04368728) objęło około 44.000 uczestników w 153 miejscach, które obejmowały liczne firmy komercyjne i ośrodki akademickie. Następnie wymieniła kilkanaście problemów, których była świadkiem, w tym:
– Uczestnicy umieszczani w korytarzu po wstrzyknięciu i nie monitorowani przez personel kliniczny.
– Brak terminowej obserwacji pacjentów, u których wystąpiły zdarzenia niepożądane.
– Niezgłaszanie odstępstw od protokołu.
– Szczepionki nie były przechowywane w odpowiedniej temperaturze
– Niewłaściwie oznakowanie próbek laboratoryjnych, oraz
– Namierzanie pracowników Ventavii za zgłaszanie tego typu problemów.
W ciągu kilku godzin Jackson otrzymała e-mail od FDA, dziękujący za jej przedstawienie swoich obaw i powiadamiając ją, że FDA nie może komentować żadnego dochodzenia, które może być wynikiem takiego zgłoszenia. Kilka dni później Brook Jackson otrzymała telefon od inspektora FDA, aby omówić jej raport, ale powiedziano jej, że żadne dalsze informacje nie mogą być dostarczone. Nie usłyszała nic więcej w związku ze swoim sprawozdaniem.
W dokumencie informacyjnym firmy Pfizer przedłożonym na spotkaniu komitetu doradczego FDA, które odbyło się 10 grudnia 2020 r. w celu omówienia wniosku firmy Pfizer o zezwolenie na zastosowanie w trybie pilnym jej szczepionki na covid-19, firma Pfizer nie wspomniała o problemach u swojego podwykonawcy [Ventavia]. Następnego dnia FDA wydała pozwolenie na dopuszczenie szczepionki do obrotu[8].
W sierpniu tego roku, po pełnym zatwierdzeniu szczepionki firmy Pfizer, FDA opublikowała podsumowanie swoich inspekcji w ramach kluczowego badania przeprowadzonego przez firmę. Skontrolowano dziewięć z 153 ośrodków badawczych. Placówki firmy Ventavia nie zostały wymienione wśród tych dziewięciu, a w ciągu ośmiu miesięcy po wydaniu zezwolenia awaryjnego w grudniu 2020 r. nie przeprowadzono żadnych inspekcji placówek, w których rekrutowano dorosłych. Urzędnik inspekcyjny FDA zauważył:
„Integralność danych i część weryfikacyjna inspekcji monitorujących badania biologiczne [BIMO] były ograniczone, ponieważ badanie było w toku, a dane wymagane do weryfikacji i porównania nie były jeszcze dostępne dla badanego nowego medykamentu”.
Relacje innych pracowników
W ostatnich miesiącach Brook Jackson ponownie zgadała się z kilkoma byłymi pracownikami Ventavii, którzy wszyscy odeszli lub zostali zwolnieni z firmy. Jeden z nich był jednym z urzędników, którzy brali udział w spotkaniu pod koniec września. W wiadomości tekstowej wysłanej w czerwcu były urzędnik przeprosił, mówiąc, że „wszystko, na co narzekałeś, było prawdą”.
Dwóch byłych pracowników Ventavii rozmawiało z czasopismem BMJ anonimowo z obawy przed odwetem i utratą perspektyw pracy w ciasno powiązanej społeczności badawczej. Obydwoje potwierdzili szerokie aspekty skargi Brook Jackson. Jedna z nich powiedziała, że pracowała nad ponad czterema tuzinami badań klinicznych w swojej karierze, w tym nad wieloma dużymi badaniami, ale nigdy nie doświadczyła takiego środowiska pracy jak w Ventavii nad badaniami Pfizera.
„Nigdy nie musiałam robić tego, o co mnie prosili, nigdy” – powiedziała BMJ. „To po prostu wydawało się czymś nieco innym niż normalnie – rzeczami, które były dozwolone i oczekiwane”.
Dodała, że podczas jej czasu w Ventavii firma oczekiwała federalnego audytu, ale ten nigdy nie nadszedł.
Drugi (były) pracownik powiedział, że po tym jak B. Jackson opuściła firmę, problemy w Ventavii utrzymywały się. W kilku przypadkach Ventavii brakowało wystarczającej ilości pracowników do zrobienia wymazu wszystkim uczestnikom badań, którzy zgłosili symptomy podobne do kowida, aby przetestować na infekcję. Laboratoryjnie potwierdzony symptomatyczny covid-19 był głównym punktem końcowym badania klinicznego, pracownik podkreślił. (Memorandum z przeglądu FDA opublikowane w sierpniu tego roku stwierdza, że w całym badaniu klinicznym wymazy nie zostały pobrane od 477 osób z podejrzanymi przypadkami objawowego covid-19).
Definicja przypadku COVID w badaniach Pfizera i Moderny
„Nie sądzę, aby to były rzetelne, czyste dane”, powiedział pracownik o danych wygenerowanych przez Ventavię w ramach badań klinicznych Pfizera. „To szalony bałagan”.
Drugi pracownik również opisał środowisko w Ventavii niepodobne do żadnego, jakiego doświadczyła w ciągu swoich 20 lat prowadzenia badań. Powiedziała czasopismu BMJ, że krótko po tym jak Ventavia zwolniła Brook Jackson, koncern Pfizer został powiadomiony o problemach w Ventavii z badaniem klinicznym szczepionki i że miał miejsce audyt.
Odkąd Brook Jackson zgłosiła problemy z Ventavią do FDA we wrześniu 2020 roku, Pfizer zatrudnił Ventavię jako podwykonawcę badań przy czterech innych badaniach klinicznych szczepionek (szczepionka Covid-19 u dzieci i młodych dorosłych, kobiet w ciąży oraz dawki przypominającej, a także badanie szczepionki RSV; NCT04816643, NCT04754594, NCT04955626, NCT05035212). Komitet doradczy przy Centers for Disease Control and Prevention ma omówić pediatryczne badanie szczepionki covid-19 w dniu 2 listopada.
Zobacz na: Transkrypt filmu ZAUFAJ WHO [Trust WHO]
Konflikt interesów. WHO i „konspiracje” związane z grypą pandemiczną – Deborah Cohen i Philip Carter
Pandemia, której nie było – dr Henry I. Miller
Dzieciom w Wielkiej Brytanii podawano toksyczne szczepionki, przyznaje firma GSK
Szkodliwa medycyna – Sprawa GlaxoSmithKline, 750 milionów dolarów kary
Szczepionka Heplisav B firmy Dynavax – adiuwant 1018 i zawały serca
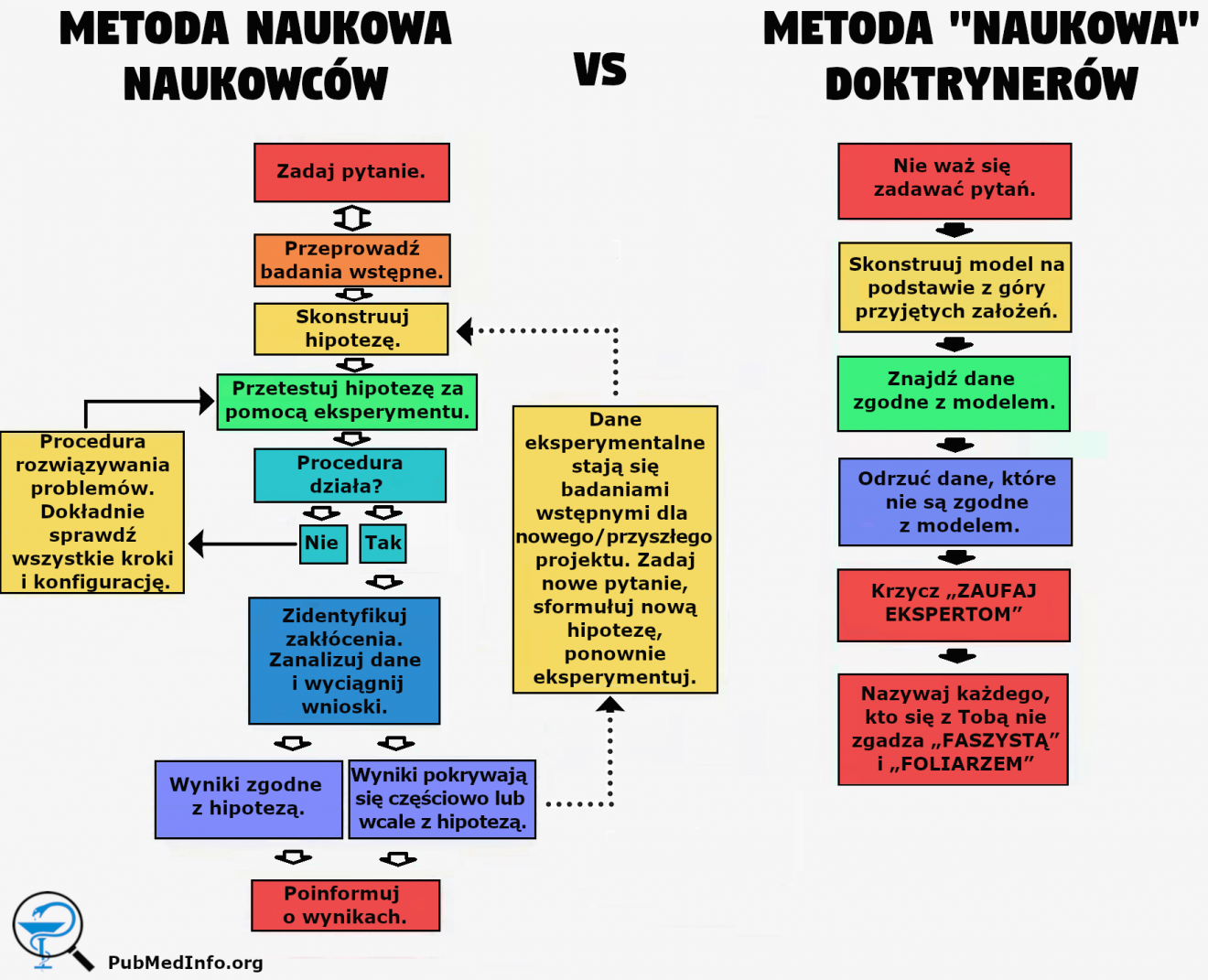
Żadna fuszerka – zamówienie było na taki właśnie wynik, więc taki jest.
wszystkie dziwne wiusy pochodzą z usa.laboratoria to- wylęgarnia.
Wyniki mają być takie, jakie zostały zamówione i opłacone. Ghost writer piszą wyniki badań na ZAMÓWIENIE, a nie takie jakie są rzeczywistości. Za duże pieniądze włożono, żeby wyszedł „zły” wynik. Wychodzi taki jaki ma być.