Mimikra molekularna pomiędzy glikoproteiną kolca SARS-CoV-2 a proteomami ssaków: poszczepienne następstwa
Źródło: Immunologic Research volume 68, pages 310–313 (2020); Molecular mimicry between SARS-CoV-2 spike glycoprotein and mammalian proteomes: implications for the vaccine

W kontekście zjawiska pod nazwą Mimikra Molekularna i reaktywności krzyżowej, warto wziąć pod uwagę kilka rzeczy:
a) przeciwciała nie są pierwszą linią obrony, a nawet niezbędnym elementem układu odpornościowego w infekcjach wirusowych (patrz agammaglobulinemia), a raczej markerem mówiącym o tym, że mieliśmy kontakt z patogenem,
b) można przejść infekcję bezobjawowo, gdy wrodzona cześć układu odpornościowego działa sprawnie, do czego jest potrzebny np. odpowiedni poziom witaminy D, albo nie przeszkadzanie organizmowi np. paracetamolem,
c) aby powstało stosunkowo dużo przeciwciał w reakcji na zastrzyk (z boskiej ambrozji), potrzeba by namnożyło się stosunkowo dużo antygenu (w tym przypadku białko kolca SARS-Cov-2) w organizmie,
d) przeciwciała to wątpliwy, a jednak chyba jedyny parametr, wokół którego kręcą się biurokraci ze służby zdrowia do mierzenia „odporności”,
e) gdy liczba przeciwciał opada, to szczepionkowi naganiacze i biurokraci ze służby zdrowia mają tylko jedno rozwiązanie tego problemu, którym są kolejne porcje boskiej ambrozji,
f) termin alergia powstał w następstwie rozpowszechnienia się na masową skalę wstrzykiwania różnego rodzaju boskich ambrozji,
g) ilość wspólnych elementów białek kolca SARS-Cov-2 produkowanych przez nasze komórki po zastrzyku z ilością elementów białek występujących w naszych organizmach, to wraz z upływem czasu i kolejnymi dawkami podtrzymującymi obecność antygenu (białko kolca SARS-Cov-2).
To do czego nieumyślnie, albo umyślnie, doprowadzą szczepionkowi naganiacze, może doprowadzić do wysypu na globalną skale problemów autoimmunologicznych. W imię próby uzyskania nieśmiertelności, osoby które poddadzą się tej eksperymentalnej terapii genowej, oprócz problemów z np. układem krwionośnym wystawiają się w dłuższym okresie czasu na problemy autoimmulogiczne, które raczej nie będą widoczne lub uciążliwe w okresie do 4 tygodni po pierwszych dwóch dawkach, kiedy to można je jeszcze zgłosić jako Niepożądany Odczyn Poszczepienny [NOP]. Nawet jeśli w twoim przypadku będzie to widoczne, to przeciętny biurokrata ze służby zdrowia i tak tego nie uzna, bo nie badano takiego zagadnienia podczas badań klinicznych, więc nie ma dowodów na związek przyczynowo skutkowy, a panujący dogmat w tej branży jest taki, że jak nie ma dowodów w postaci badań opisujących dany problem zdrowotny to znaczy że jako lekarz można mówić, że nie istnieje taki problem.
SARS-CoV-2 w kontekście patentów sprzed 20 lat – dr David Martin
Dossier na temat Anthony Fauciego/COVID-19 – dr David Martin
Potencjalne problemy autoimmunologiczne i neurodegeneracyjne szczepionek na Covid-19 – Dr Christopher Shaw
Potencjalna antygenowa reaktywność krzyżowa pomiędzy SARS-CoV-2 a tkankami ludzkimi z możliwym związkiem ze wzrostem zachorowań na choroby autoimmunologiczne
Słowa Alergia i Anafilaksja zostały utworzone, aby opisać szkody po szczepionkach
Dr Peter McCullough o blokowaniu metod leczenia Covid-19
Mimikra molekularna pomiędzy glikoproteiną kolca SARS-CoV-2 a proteomami ssaków: poszczepienne następstwa
Etiopatologia choroby wywołanej zakażeniem SARS-CoV-2 u gospodarza ludzkiego[1] jest przedmiotem intensywnych badań. Prawdopodobnym mechanizmem jest to, że mnogość chorób wchodzących w skład COVID-19 wynika ze zjawisk mimikry molekularnej pomiędzy białkami wirusa i człowieka[2]. Racjonalnym uzasadnieniem jest to, że po zakażeniu reakcje immunologiczne wywołane przeciwko patogenowi mogą reagować krzyżowo z białkami ludzkimi, które mają wspólne sekwencje (lub struktury) peptydowe z patogenem, prowadząc w ten sposób do szkodliwych patologii autoimmunologicznych[3, 4]. Z tego powodu, dysfunkcje płuc i dróg oddechowych związane z zakażeniem SARS-CoV-2 mogłyby być tłumaczone współdzieleniem peptydów pomiędzy glikoproteiną kolca SARS-CoV-2 a białkami surfaktantu pęcherzykowego płuc[2]. Na poparcie tej tezy w kolejnych raportach[5,6,7,8] podkreśla się, że mimikra molekularna i reaktywność krzyżowa mogą wyjaśniać choroby wywoływane przez SARS-CoV. Co szczególnie interesujące, sugeruje się również krzyżowe rozpoznawanie limfocytów T pomiędzy krążącymi koronawirusami „przeziębienia” i SARS-CoV-2[9].
[Mimikra molekularna jest definiowana jako teoretyczna możliwość, że podobieństwo sekwencji pomiędzy peptydami obcymi i własnymi jest wystarczające, aby doprowadzić do krzyżowej aktywacji autoreaktywnych limfocytów T lub B przez peptydy pochodzące od patogenu – Wiki]
[Peptydy to krótkie łańcuchy aminokwasów połączone wiązaniami peptydowymi. Łańcuchy składające się z mniej niż dziesięciu lub piętnastu aminokwasów nazywane są oligopeptydami i obejmują dipeptydy, tripeptydy i tetrapeptydy – Wiki]
[Proteom (z połączenia słów proteina i genom) – zestaw białek występujących w komórce w danym momencie, białkowy odpowiednik genomu – Wiki]
W tych ramach naukowych, niniejsze badanie przeanalizowało w sposób porównawczy współdzielenie peptydów między SARS-CoV-2 a gatunkami ssaków. Nasze rozumowanie jest takie, że jeśli prawdą jest, że mimikra molekularna pomiędzy SARS-CoV-2 i ludzkimi białkami przyczynia się do lub wywołuje COVID-19, wówczas różne poziomy/wzory mimikry molekularnej w porównaniu do wirusa powinny charakteryzować różne gatunki zwierząt. Rzeczywiście, istnieje niewiele danych wskazujących, że zwierzęta domowe, na przykład psy i koty, mogą przenosić wirusa lub rozwijać sieć chorób związaną z wirusem[10]. Ogólnie rzecz biorąc, obecnie panuje zgoda co do tego, że nie ma dowodów na to, że zakażone zwierzęta domowe są źródłem zakażenia SARS-CoV-2 dla ludzi lub innych zwierząt domowych[11, 12].
Opierając się na tych przesłankach i wykorzystując heksa- i heptapeptydy jako próbki sekwencji[13,14,15], przeanalizowano nakładanie się peptydów między glikoproteiną kolca SARS-CoV-2 a proteomami ssaków.
Metody
Analizy dotyczące współdzielenia peptydów zostały obszernie opisane gdzie indziej[16, 17]. W skrócie, pierwotna sekwencja glikoproteiny kolca SARS-CoV-2 (NCBI białko Id=QHD43416.1) została podzielona na heksa- i heptapeptydy przesunięte o jedną resztę (tj. MFVFLV, FVFLVL, VFLVLL, FLVLLP). Otrzymano 1268 heksapeptydów i 1267 heptapeptydów. Następnie każdy wirusowy heksa- lub heptapeptyd był analizowany jako próbka do przeszukania pod kątem występowania tego samego heksa- lub heptapeptydu w proteomie referencyjnym z następujących ssaków (z identyfikatorem taksonomii w nawiasie): człowiek, Homo sapiens (9606); mysz, Mus musculus (10090); szczur, Rattus norvegicus (10116); kot, Felis catus (9685); pies, Canis lupus familiaris (9615); królik, Oryctolagus cuniculus (9986); szympans, Pan troglodytes (9598); goryl, Gorilla gorilla gorilla (9595); i makak królewski, Macaca mulatta (9544). Trzy proteomy wirusowe zostały dodane jako środki kontroli koronawirusów: ludzki koronawirus HKU1 (290028); ludzki koronawirus 229E (11137); i ludzki koronawirus OC43 (31631). Analizy dopasowania heksa/heptapeptydów przeprowadzono przy użyciu programu Pir Peptide Matching[18].
Wartość oczekiwana dla współdzielenia heksapeptydów przez dwa białka została obliczona poprzez rozważenie liczby wszystkich możliwych heksapeptydów. Jako że w heksapeptydzie każda reszta może być dowolnym z 20 aminokwasów (aa), liczba wszystkich możliwych heksapeptydów N jest dana przez N = 206 = 64 × 106. Następnie, liczba oczekiwanych wystąpień jest wprost proporcjonalna do liczby heksapeptydów w obu białkach i odwrotnie proporcjonalna do N. Zakładając, że liczba heksapeptydów w obu białkach wynosi << N i lekceważąc względną liczebność aa, otrzymujemy wzór wyprowadzony w przybliżeniu, gdzie oczekiwana liczba heksapeptydów wynosi 1/N lub 20-6. Stosując te same obliczenia, oczekiwana wartość dla współdzielenia heptapeptydów przez dwa białka jest równa 20-7.
Wyniki
Graficzną ilustrację współdzielenia peptydów między glikoproteiną kolca SARS-CoV-2 a analizowanymi proteomami ssaków i koronawirusów przedstawiono na Ryc. 1. Sekwencje heksa- i heptapeptydowe biorące udział we współdzieleniu zostały wyszczególnione odpowiednio w Tabelach S1 i S2.
.
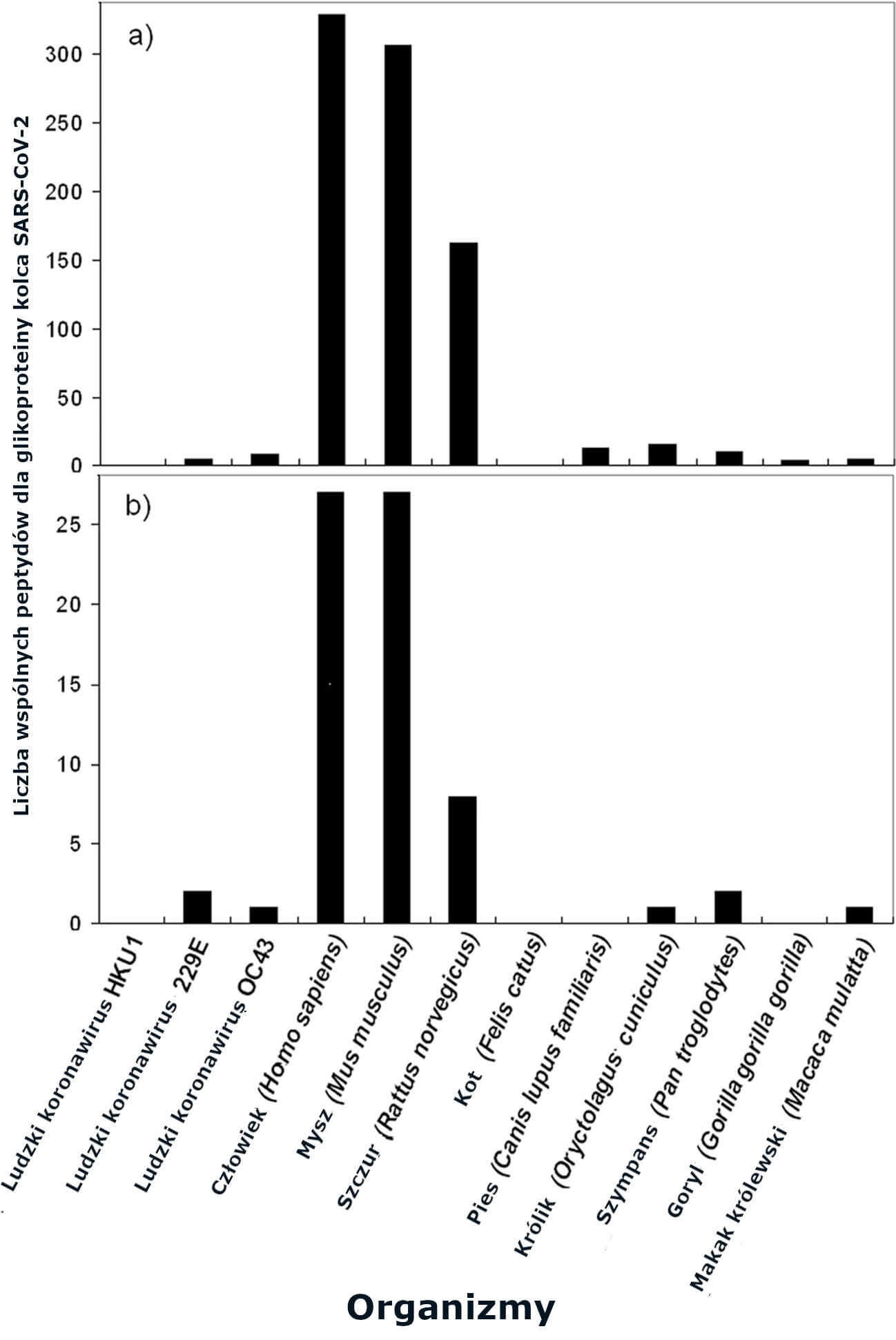
Współdzielenie peptydów pomiędzy glikoproteiną kolca SARS-CoV-2 a proteomami ssaków i koronawirusów. a Współdzielenie peptydów na poziomie 6-mer. b Współdzielenie peptydów na poziomie 7-mer
Rycina 1 pokazuje, że:
- Między glikoproteiną kolca SARS-CoV-2 a białkami ludzkimi istnieje duże współdzielenie heptapeptydów. Takie pokrywanie się peptydów jest nieoczekiwane i wysoce nieprawdopodobne z matematycznego punktu widzenia, biorąc pod uwagę, że, jak wyszczególniono w rozdziale „Metody”, prawdopodobieństwo wystąpienia w dwóch białkach tylko jednego heptapeptydu jest równe ~ 20-7 (lub 1 na 1.280 000.000). Podobnie, prawdopodobieństwo wystąpienia w dwóch białkach tylko jednego heksapeptydu jest bliskie zeru i wynosi ~ 20-6 (lub 1 na 64.000.000).
- Jedynie współdzielenie się peptydami wirusowymi z proteomem myszowatych i, w mniejszym stopniu, z proteomem szczurów dotrzymuje kroku temu, co wykazują białka ludzkie;
- Zwierzęta domowe, królik i trzy analizowane tu naczelne nie mają żadnych lub tylko kilka wspólnych peptydów;
- Podobnie, proteomy trzech ludzkich koronawirusów HKU1, 229E i OC43, które były używane jako wirusowe środki kontrolne, nie mają żadnych lub tylko kilka peptydów wspólnych z glikoproteiną kolca. Pod tym względem wydaje się, że glikoproteina kolca SARS-CoV-2 jest fenetycznie bardziej podobna do ludzi i myszy niż do swoich „kuzynów” koronawirusów.
[Fenetycznie – odnoszący się do lub oznaczający system klasyfikacji organizmów oparty na analizie dużej liczby policzalnych charakterystycznych cech, bez uwzględnienia relacji ewolucyjnych.]
Wnioski
Badanie to dokładnie określa ilościowe współdzielenie z proteomami ssaków heksa- i heptapeptydów glikoproteiny kolca SARS-CoV-2, która jest głównym antygenem wirusa. Duża wspólność peptydów występuje u ludzi i myszy, czyli u organizmów, które ulegają patologicznym następstwom po zakażeniu SARS-CoV-2. Natomiast u ssaków, które nie mają poważnych patologicznych następstw po zakażeniu SARS-CoV-2, nie występują żadne wspólne peptydy lub występują w niewielkiej liczbie[10,11,12]. Z tego powodu dane te wydają się być niepodważalnym dowodem na korzyść mimikry molekularnej jako potencjalnego mechanizmu, który może przyczyniać się do lub wywoływać choroby związane z SARS-CoV-2[8].
Drugą istotną uwagą jest to, że badanie to wskazuje na konieczność poświęcenia szczególnej uwagi wyborowi zwierząt laboratoryjnych, które mają być wykorzystane w badaniach przedklinicznych podczas formułowania/zatwierdzania szczepionek przeciw patogenom. W omawianym przypadku, biorąc pod uwagę najniższy poziom podobieństwa sekwencji glikoproteiny kolca SARS-CoV-2 w stosunku do białek naczelnych, wyniki uzyskane w badaniach wykorzystujących naczelne jako modele zwierzęce, tj. makaka królewskiego[19], byłyby niewiarygodne ze względu na brak możliwości weryfikacji występowania reaktywności krzyżowej i związaną z nią autoagresją przy braku wspólnych sekwencji. Pod tym względem, dane zilustrowane na Ryc. 1 wyjaśniają, dlaczego, jak podkreślił Hogan[20], „zakażenie SARS-CoV makaków krabożernych nie odtworzyło ciężkiego przebiegu choroby obserwowanego w większości przypadków SARS u dorosłych ludzi”[21]. W rzeczywistości, w badaniu, w którym zarówno makaki królewskie, jak i krabożerne zostały zakażone SARS-CoV, nie zaobserwowano żadnych objawów klinicznych choroby ani wyraźnej patologii płuc[22], a wniosek autorów jest taki, że model makaka ma ograniczoną przydatność w badaniach nad SARS i ocenie terapii. W ten sam sposób McAuliffe i in.[23] opisali podobne wyniki badań: „SARS-CoV podany donosowo i dotchawiczo makakom królewskim, krabożernym i kotawcom zielonosiwym replikował się w drogach oddechowych, ale nie wywoływał choroby”.
Jeśli chodzi o zwierzęta domowe i bydło, koronawirusy są od dawna znane jako patogeny jelitowe kotów (FeCoV), psów (CaCoV), bydła (BCoV) i świń (TGEV)[24]. Niemniej jednak, koronawirusy nie wydają się być chorobotwórcze dla zwierząt domowych i bydła. Rzeczywiście, znikoma lub zerowa podatność na patologie wywołane przez SARS-CoV-2 jest poświadczona przez American Veterinary Medical Association, które dosłownie oświadcza:
„w ciągu pierwszych pięciu miesięcy epidemii COVID-19 (1 stycznia – 8 czerwca 2020), co obejmuje pierwsze dwanaście tygodni po ogłoszeniu 11 marca przez WHO globalnej pandemii, mniej niż 20 zwierząt domowych uzyskało pozytywny wynik testu na SARS-CoV-2, z potwierdzeniem, na całym świecie. I to pomimo faktu, że na dzień 8 czerwca liczba osób, u których potwierdzono obecność COVID-19 przekroczyła 7 milionów na świecie i 1,9 miliona w Stanach Zjednoczonych” (https://www.avma.org/).
Podsumowując, w świetle danych przedstawionych na Ryc. 1 oraz biorąc pod uwagę parametry podatności, takie jak starzenie się i stan zdrowia, jedynie starzejące się myszy wydają się być prawidłowym modelem zwierzęcym do testowania szczepionki przeciw SARS-CoV-2 zawierającą gen kodujący glikoproteinę kolca, która ma być stosowana u ludzi[25, 26].
Wreszcie, niniejsze badanie po raz kolejny potwierdza koncepcję, że tylko szczepionki oparte na minimalnych immunologicznych czynnikach warunkujących unikalnych dla patogenów i nieobecnych w ludzkim proteomie mogą oferować opcję bezpiecznych i skutecznych szczepionek[16, 27,28,29,30].