Ciąża, Odporność, Schizofrenia i Autyzm – dr Paul Patterson
Źródło: Patterson, Paul H. (2006) Pregnancy, Immunity, Schizophrenia, and Autism. Engineering & Science 69 (3). 2006, pp. 10-21.
http://calteches.library.caltech.edu/4166/

Kuszenie św. Antoniego namalowane przez Hieronima Boscha znajdujący się obecnie w Narodowym Muzeum Sztuki Dawnej w Lizbonie. Fantastyczne – w najściślejszym znaczeniu tego słowa – figury przedstawione tutaj są podobne do niektórych halucynacji zgłaszanych przez osoby cierpiące na schizofrenię.
Ciąża, Odporność, Schizofrenia i Autyzm – dr Paul Patterson
Czy coś tak niegroźnego jak grypa może powodować schizofrenię? Czy lekki katar ciężarnej mamy może mieć konsekwencje na całe życie dla jej nienarodzonego dziecka? Czy własny układ odpornościowy mózgu odgrywa rolę w autyzmie? Odpowiedzi na te i pokrewne pytania są rzeczywiście zaskakujące i mogą sugerować nowe możliwości leczenia, a nawet zapobiegania.
W miarę jak dowiadujemy się więcej o powiązaniach między mózgiem a układem odpornościowym, odkrywamy, że te pozornie niezależne sieci komórek w rzeczywistości ciągle rozmawiają ze sobą. U dorosłego, aktywacja układu odpornościowego powoduje wiele uderzających zmian w zachowaniu – zwiększona ilość snu, utrata apetytu, mniej interakcji społecznych – i, oczywiście, bóle głowy. Z kolei, stres w twoim życiu (postrzegany przez mózg) może wpływać na funkcję odpornościową – mózg reguluje narządy odpornościowe, takie jak śledziona, poprzez autonomiczny układ nerwowy.
Ostatnie dowody wskazują, że ta rozmowa między mózgiem a układem odpornościowym faktycznie rozpoczyna się podczas rozwoju zarodka, gdzie stan układu odpornościowego matki może zmieniać wzrost komórek w mózgu płodu. Jak zobaczymy, takie zmiany mogą prowadzić do zwiększonego ryzyka schizofrenii lub autyzmu u potomstwa.
Najpierw rozważmy schizofrenię, która jest zaburzeniem progresywnym, którego początkowe objawy psychotyczne pojawiają się zwykle we wczesnej dorosłości. (Chwytliwe przedstawienie tego, jak u cierpiącego mogą wyglądać epizody psychotyczne, patrz Russell Crowe w filmie Piękny umysł.) Ludzie ze schizofrenią mogą wydawać się całkiem normalni przez pewien okres czasu, a następnie mają bardzo poważne problemy, co jest dla nich ogromną trudnością – ludzie zwykle obwiniają ofiarę i zastanawiają się, dlaczego pacjent się nie ogarnie i nie zachowuje się prawidłowo.
W ostatnim dziesięcioleciu zaczęły się pojawiać anatomiczne i funkcjonalne różnice między mózgami schizofrenicznymi i typowymi. Obrazowanie metodą rezonansu magnetycznego (MRI) mózgu identycznych bliźniaków, jednego ze schizofrenią, a drugiego bez, wykazało, że w 90 procentach przypadków bliźniak ze schizofrenią ma powiększone komory, które są w kształcie motyla, puste przestrzenie w centrum mózgu wypełnione płynem mózgowo-rdzeniowym. Jednym z wyjaśnień tego rozszerzenia jest to, że szara materia otaczająca komory mogła się skurczyć, co oznacza, że mózg ma lub może mieć mniej neuronów. Lub neurony mogą być bardziej gęsto upakowane. Alternatywna hipoteza bierze pod uwagę infekcję – na przykład zapalenie mózgu rozszerzy komory. Schizofrenia nie jest wynikiem samej infekcji dojrzałego mózgu, ale istnieją inne przesłanki, do których wrócę, że infekcje mogą odgrywać rolę na bardzo wczesnym etapie życia.
Badanie MRI pokazuje szczegóły anatomiczne, ale funkcjonalne MRI, które śledzi przepływ krwi, pokazuje aktywność mózgu. Im więcej krwi przepływa przez określoną część mózgu, tym bardziej prawdopodobnie jest ona aktywna. W tych prezentacjach funkcjonalnych skanów MRI chorego na schizofrenię głowa po lewej stronie pokazuje na żółto, że kora słuchowa świeci się, gdy przez słuchawki odtwarzany jest dźwięk stereofoniczny. Druga głowa pokazuje aktywność mózgu, gdy pacjent naciska przycisk, aby zasygnalizować, że „słyszy głosy”. Halucynacje [omamy] pojawiają się tylko w dominującej półkuli, więc u tego pacjenta praworęcznego świeci tylko kora słuchowa lewej półkuli. Mówiono kiedyś, że głosy w ich głowach były wyobrażone, ale ponieważ w tej części mózgu występuje aktywność, która faktycznie przetwarza informacje słuchowe, w pewnym sensie naprawdę istnieją. Schizofrenicy słyszą dźwięki, przynajmniej ich mózgi, i bardzo interesujące byłoby odkrycie, co generuje tę aktywność spontanicznie.
Wiemy, że schizofrenia zaczyna się na wczesnym etapie rozwoju. Statystycznie dzieci, u których później rozwija się psychoza, są bardziej podatne na problemy dyscyplinarne w szkole, mają zwykle niższy iloraz inteligencji i są bardziej narażone na problemy emocjonalne i społeczne. Różnice są zbyt małe, aby były przydatne do wczesnej diagnozy, ale już istnieją. Występuje również zaskakujące opóźnienie w rozwoju funkcji motorycznych – siedzenia, stania, chodzenia i tak dalej.
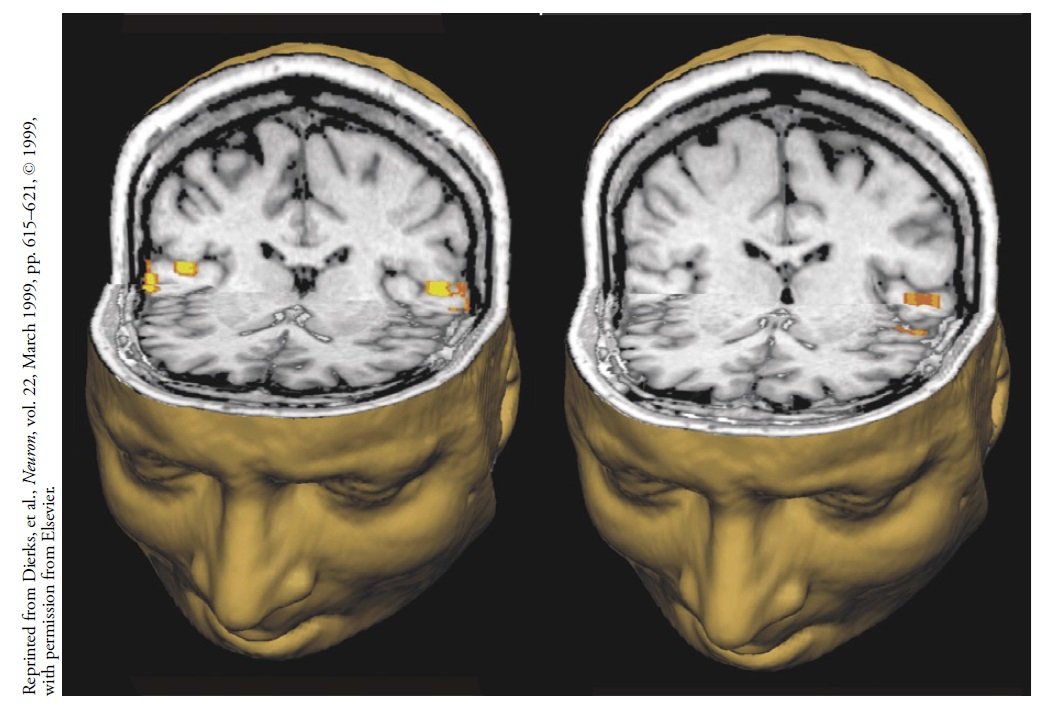
Zakręty Heschla są głównym ośrodkiem przetwarzania dźwięku w mózgu. Prawdziwy dźwięk rozświetla go po obu stronach mózgu, jak widać po lewej stronie tych trójwymiarowych odwzorowań. Zakręt świeci spontanicznie podczas halucynacji słuchowej (po lewej), ale tylko po dominującej stronie mózgu.
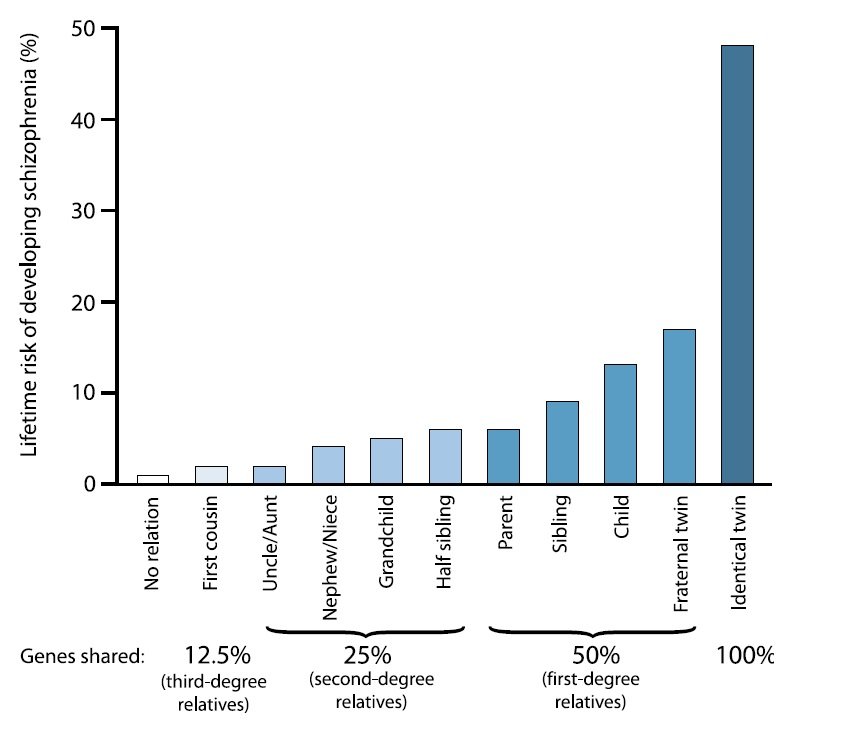
Wyraźnie istnieje genetyczna predyspozycja do schizofrenii. Ta tabela pokazuje, jak zwiększa się ryzyko rozwoju choroby, jeśli mam bliskiego krewnego ze schizofrenią – im więcej [ekspresji] genów dzielisz z chorą osobą, tym większa twoja podatność. Zaczerpnięte z Schizophrenia Genesis: The Origins of Madness by Irving I. Gottesman, W. H. Freeman and Company, New York, 1990

Rozdzieleni przy porodzie, bliźniacy Mallifert spotkali się przypadkowo.
Schizofrenia ma komponent genetyczny. Najważniejszym czynnikiem ryzyka do przewidywania schizofrenii jest rodzeństwo z zaburzeniem. W populacji ogólnej ryzyko schizofrenii wynosi około 1 procent na całym świecie. Jeśli masz schizofrenicznego kuzyna, wujka lub ciotkę, ryzyko jest podwojone, co nie jest bardzo znaczące. Ale jeśli masz identycznego bliźniaka ze schizofrenią, ryzyko wynosi około 50 procent, że staniesz się również schizofrenikiem. Ale to nie jest 100 procent, więc nie jest to klasyczna, dominująca choroba genetyczna, taka jak choroba Huntingtona, w której pojedynczy nieprawidłowo działający gen powoduje zaburzenie. Ludzie uważają raczej, że w grę wchodzi około 6–12 genów, z których każdy wiąże się z niewielkim ryzykiem. W ciągu ostatnich kilku lat zidentyfikowano szereg tych genów, w tym neuregulinę, dysbindynę i jeden zwany “Disrupted-in-Schizophrenia [zaburzony w schizofrenii]” lub DISC1. Co więcej, każdy z tych genów jest dobrze znany z badań na zwierzętach jako bardzo ważny we wczesnym rozwoju embrionalnego mózgu.
Istnieje również komponent ryzyka środowiskowego. Urodzenie się w miesiącach zimowych lub wiosennych lub urodzenie i wychowanie w mieście zwiększają ryzyko. Jest to zgodne z zakaźną hipotezą – częściej chorujemy zimą i wiosną, a także częściej stykami się z zarazkami innych ludzi, jeśli mieszkamy w zatłoczonym obszarze.
Innym ważnym czynnikiem ryzyka środowiskowego jest infekcja u matki, która będzie jednym z moich głównych tematów. Infekcja układu oddechowego w drugim trymestrze ciąży zwiększa ryzyko schizofrenii u potomstwa. W 2000 roku Alan Brown i jego koledzy z Columbia University w Nowym Jorku przestudiowali dokumentację medyczną 12.000 kobiet w ciąży, które należały do Kaiser HMO w okolicach Oakland. Alan Brown stwierdził, że ryzyko zwiększało się trzykrotnie jeśli wystąpiła infekcja układu oddechowego w drugim trymestrze ciąży, co potwierdza wnioski z poprzednich badań, w których badacze nie mieli dostępu do dokumentacji pacjenta. Następnie naukowcy przeanalizowali zamrożone próbki surowicy od tych kobiet i stwierdzili podobne, a nawet większe – aż siedmiokrotnie – zwiększone ryzyko, jeśli przeciwciała przeciw grypie były obecne w pierwszej połowie ciąży. Co więcej, znaleźli statystycznie istotny związek z podwyższonymi poziomami niektórych członków grupy białek zwanych cytokinami. Cytokiny są wytwarzane przez białe krwinki, a ich poziom we krwi wzrasta, gdy pojawi się infekcja. Obliczenie tak zwanego możliwego do przypisania ryzyka na podstawie tych danych doprowadziło do oszacowania, że około 20 procent przypadków schizofrenii nie wystąpiłoby, gdyby zapobiec ekspozycji na grypę.
To naprawdę dramatyczna informacja, szczególnie biorąc pod uwagę, że naukowcy musieli całkowicie zignorować obszar genetyczny. (Nawet teraz nie możemy badać w celu wykrycia genów podatności, które zostały zidentyfikowane.) Zatem badanie prawdopodobnie obejmowało dużą liczbę osób, które nigdy nie chorują na schizofrenię, ponieważ nie są genetycznie predysponowane, a mimo to znaleziono trzy do siedmiokrotny wzrost ryzyka. Rzeczywiste ryzyko infekcji u matki prawdopodobnie będzie zatem znacznie wyższe.
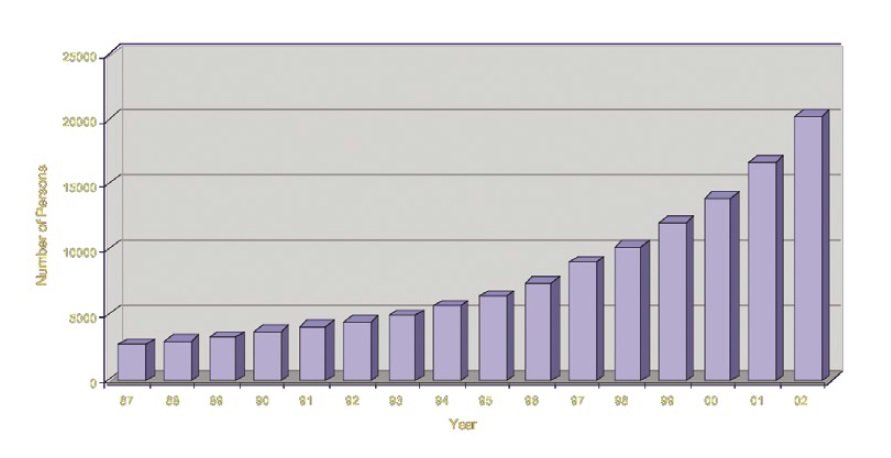
Ten wykres pokazuje, roczną liczbę osób ze zdiagnozowanym autyzmem, które były obsługiwane przez Kalifornijski Department of Developmental Services, liczby gwałtownie wzrosły w połowie lat 90.
Inne badania na dorosłych osobach schizofrenicznych wykazały brak równowagi cytokin i podwyższony poziom białych krwinek we krwi. A leki przeciwpsychotyczne, takie jak klozapina, które ludzie przyjmują w celu leczenia halucynacji i nieuporządkowanych myśli, są znane z badań na zwierzętach w celu modulowania poziomu cytokin we krwi. Leki te mogą więc działać nie tylko w mózgu, ale także na niektóre aspekty układu odpornościowego, aby osiągnąć ich skuteczność. Myślę, że jest to bardzo interesujące spostrzeżenie, ale nie zrobiło jeszcze większego wrażenia na społeczności badawczej, więc nie zbadano dokładnie tej możliwości.
Zapalenie mózgu cechą autyzmu, wykazują wyniki badania z Johns Hopkins University
Niedawny, bardzo imponujący artykuł Williama Eatona i współpracowników z Johns Hopkins University Medical School przeanalizował niezwykle kompleksowe zapisy systemu opieki zdrowotnej w Danii, który śledzi każdego Duńczyka od kołyski aż po grób. Badacze mieli dostęp do akt wszystkich 7.704 osób, u których zdiagnozowano schizofrenię w latach 1981–1998, w tym do szczegółów każdej wizyty w szpitalu. Okazuje się, że u osób, które rozwinęły którekolwiek z dziewięciu różnych zaburzeń autoimmunologicznych – schorzeń, w których układ odpornościowy organizmu zaczyna atakować własne komórki – ryzyko wystąpienia schizofrenii wzrosło o 45 procent.
Istnieje więc związek między układem odpornościowym a schizofrenią, ale nie wiemy, co to jest. Wiemy, że istnieje genetyczna predyspozycja do choroby autoimmunologicznej – czy geny odpowiedzialne za tę predyspozycję są w jakiś sposób powiązane z genami predysponującymi do schizofrenii? Czy może chodzi o coś z zaburzeniami autoimmunologicznymi, takimi jak tworzenie przeciwciał przeciwko niektórym cząsteczkom, co zwiększa ryzyko schizofrenii?
Teraz przejdźmy do autyzmu, który pierwotnie został opisany przez Leo Kannera z Johns Hopkins w 1943 roku jako rodzaj schizofrenii. Nie myślimy już dłużej w ten sposób, ale istnieją pewne interesujące podobieństwa – szczególnie w wycofywaniu pacjentów z otaczającego ich świata. [Ciąża, Odporność, Schizofrenia i Autyzm]
Cechami charakterystycznymi autyzmu są oczywiście niewystarczające umiejętności społeczne – pacjenci nie czytają dobrze emocji innych ludzi lub nie odpowiednio na nie reagują – oraz brak rozwoju mowy. Z przykrością stwierdza się, że około 30 procent pacjentów faktycznie odczuwa regresję w tych obszarach, która zaczyna się w wieku około trzech lat. Jednak w przeciwieństwie do schizofreników dzieci autystyczne często wykazują dziwne, powtarzające się gesty – uderzanie głową o ścianę lub trzepotanie rękami, co jest klasycznym objawem często stosowanym przez nauczycieli jako możliwym wskazaniem, że może istnieć problem. Osoby autystyczne mają tendencję do skupiania się na przedmiotach i rytuałach. Pacjent może spędzać godziny na zabawie np. kawałkiem sznurka lub zjedzeniem obiadu we właściwy sposób. Istnieje również lęk przed nowymi sytuacjami lub przedmiotami, a często znaczne problemy z bodźcami czuciowymi – na przykład ekstremalna wrażliwość na dźwięki. Niepokojące wydaje się, że liczba przypadków autyzmu gwałtownie rośnie. Jednak nie jest jasne, ile z tego faktycznie stanowi wzrost częstości występowania autyzmu lub wzrost diagnozy autyzmu, a nie na przykład upośledzenie umysłowe.
Podobnie jak w przypadku schizofrenii, autyzm ma silny genetyczny komponent – jedynym największym czynnikiem ryzyka jest rodzeństwo. Autyzm jest również zaburzeniem multi genetycznym, w którym uczestniczy sześć do 10 genów, i ponownie, geny, które do tej pory zostały zidentyfikowane (neuroliginy 3 i 4, En-2 i Hox-a1) są bardzo ważne w rozwoju zarodkowego mózgu. Ponadto istnieją czynniki środowiskowe związane z ryzykiem wystąpienia autyzmu. Kwas walproinowy, który jest stosowany w leczeniu padaczki, powoduje dramatyczny wzrost ryzyka autyzmu, gdy kobiety przyjmują go, zanim dowiedzą się, że są w ciąży. Ten lek jest nadal powszechnie przepisywany, ale ludzie zaczynają martwić się jego stosowaniem przez kobiety w ciąży.
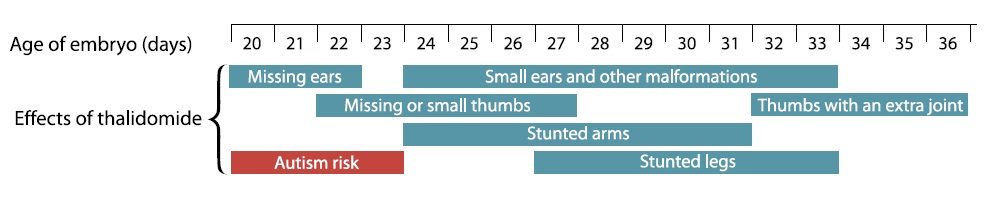
Palce u rąk i nóg, kończyny i narządy rozwijają się u płodu zgodnie z bardzo ścisłym harmonogramem, a rodzaje wad wrodzonych obserwowane u dzieci wystawionych na działanie talidomidu korelują bardzo dokładnie z momentem, kiedy matka przyjmowała medykament. Niektóre dzieci po talidomidzie są również autystyczne, co ujawnia okno podatności na zagrożenia we wczesnym rozwoju mózgu. Dane dotyczące autyzmu za K. Strömland i in. z Developmental Medicine and Child Neurology, kwiecień 1994; grafika za Patricią Rodier, Scientific American, luty 2000
Mamy cenny wgląd w okres podatności płodu dzięki tragedii związanej ze stosowaniem talidomidu. Ci z was, którzy są wystarczająco starzy, pamiętają stosowanie talidomidu jako leku przeciw porannym mdłościom w latach 60. W następstwie jego stosowania powstały poważne wady wrodzone, podobnie jak zwiększona zapadalność na autyzm. Ale kluczowe jest tutaj to, że rodzaj nieprawidłowości fizycznych – brakujące uszy, skrócone ręce, lub nogi – zależał od tego, na jakim etapie ciąży była matka. Innymi słowy, deformacja dziecka mówiła nam dokładnie, kiedy, czasami w ciągu jednego lub dwóch dni, matka zażyła lek. Okazało się, że okno ryzyka autyzmu przypada na dni od 20 do 23 po zapłodnieniu – bardzo wczesny etap rozwoju neuronów. W tym momencie cewa nerwowa właśnie się zamyka i tworzą się pierwsze neurony. Podobne okno ryzyka występuje w przypadku kwasu walproinowego i leku zapobiegającego wrzodom zwanego mizoprostolem. W większości przypadków nie znamy przyczyny lub przyczyn autyzmu, ale to okno podatności na zagrożenia jest wyraźnie bardzo ważną wskazówką, jak mózg ulega zmianie w tym zaburzeniu.
Ponownie, podobnie jak w schizofrenii, istnieje czynnik ryzyka związany z infekcją u matki. W przeglądzie literatury Andrei i Rolanda Ciaranello z Stanford autorzy stwierdzili, że „główną niegenetyczną przyczyną autyzmu jest prenatalna infekcja wirusowa”. Twierdzenie to opierało się głównie na badaniach epidemii różyczki w stanie Nowa Anglia w 1964 roku. 10 procent dzieci urodzonych przez matki chorujące na różyczkę w czasie ciąży wykazywały objawy autyzmu, co jest astronomicznym wzrostem ryzyka. Oczywiście różyczka nie jest już powszechna, ponieważ jesteśmy zaszczepieni przeciwko niej, ale chodzi o to, że infekcja u matki może zwiększyć ryzyko autyzmu. W grę wchodzą także inne infekcje – w zeszłym tygodniu ukazał się artykuł łączący infekcję opryszczki narządów płciowych ze zwiększonym ryzykiem autyzmu.
Bez wchodzenia w szczegóły odsetek chorób autoimmunologicznych i alergii jest wyższy w rodzinach z autyzmem, szczególnie u matki. Istnieją również doniesienia o zaburzeniach odporności we krwi osób z autyzmem. Te różne połączenia z układem odpornościowym przypominają oczywiście schizofrenię.
Istnieją również bardzo uderzające dowody na rozregulowanie układu odpornościowego w samym mózgu. W zeszłym roku grupa prowadzona przez Carlosa Pardo z Johns Hopkins znalazła coś, co nazywają „zapaleniem nerwów” w pośmiertnym badaniu mózgów pacjentów z autyzmem, którzy zmarli w wieku od ośmiu do 44 lat. Ale ci ludzie nie przechodzili infekcji w chwili śmierci – zmarli z takich powodów jak utonięcie lub zawał serca. Badanie wykazało, że komórki mikrogleju, które działają jak własny układ odpornościowy mózgu, były aktywowane.
Badanie wykazało także niesamowity wzrost niektórych cytokin w mózgu i innych w płynie mózgowo-rdzeniowym. W mojej opinii jest to przełomowy artykuł. Jest to pierwszy dowód na to, że w mózgach osób z autyzmem trwa ciągła aktywacja układu odpornościowego. Jest to stan subkliniczny, ponieważ nie ma jawnej infekcji. Ale tam jest.
Aby spróbować rozwikłać, w jaki sposób układ odpornościowy jest powiązany z rozwojem tych chorób, zwróciliśmy się do modelu zwierzęcego. Zwierzęta są niezbędne dla postępu medycznego. Jeśli uważasz, że gen jest istotny w danej chorobie, możesz wprowadzić ten gen do myszy i sprawdzić, czy rozwinie się coś w rodzaju ludzkiej choroby. Możesz także przetestować bakterie, wirusy i toksyny środowiskowe. Możesz badać patogenezę – jak postępują stadia choroby i jak rozprzestrzenia się z tkanki na tkankę – u zwierząt o wiele łatwiej niż u ludzi. I oczywiście możesz testować leczenie. Zgodnie z prawem musisz najpierw przetestować leki na zwierzętach. W ten sposób opracowujemy szczegóły nowych procedur chirurgicznych i badamy potencjał nowych terapii, na przykład dotyczących komórek macierzystych. Bez poprzedzających je badań na zwierzętach takie powszechne, ale bardzo złożone procedury, takie jak przeszczep szpiku kostnego, nerek i serca, nie byłyby dziś dostępne.
Prawda o komórkach macierzystych – wywiad z dr Theresą Deisher
Film WIWISEKCJA – Śmiertelna medycyna [1997]
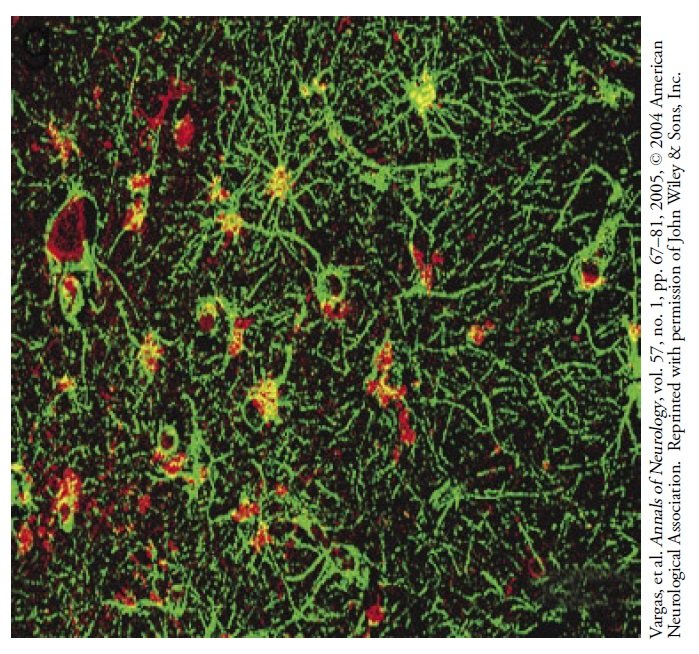
W tym przekroju móżdżku pacjenta z autyzmem komórki mikrogleju zostały aktywowane, o czym świadczy ich wchłanianie czerwonego barwnika, który wiąże się z białkiem układu odpornościowego zwanym HLA-DR.
To wszystko piękne i ładne, ale co ze zwierzęcymi modelami chorób psychicznych? Jak poddać psychoanalizie mysz? Jak rozpoznać, czy ma halucynacje? (Wydaje mi się, że możemy, ale to temat na osobny wykład). A w jaki sposób modelujemy chorobę taką jak autyzm, która podobno wyjątkowo ma występować tylko u ludzi? Jak zmierzyć upośledzenie umiejętności językowych autystycznej myszy, gdy – przepraszam, Walt – przede wszystkim trzeba zacząć od tego, że nie są w stanie mówić? A przynajmniej nie rozumiemy tej mysiej mowy – komunikują się za pośrednictwem wezwań alarmowych. Istnieją nawet spekulacje, że potrafią rozpoznać inne myszy na podstawie ich głosu. Ale to znowu inna historia.
Na szczęście tak nie jest w przypadku modeli zwierzęcych. Nie naśladujemy całej choroby w żadnym modelu – naśladujemy jej cechy. Mogą to być np. umierające neurony. Może to być zmiana właściwości elektrycznych neuronów lub zmiana molekularna, taka jak poziom cytokin. Lub może to być drżenie albo zaciąganie nogami w chorobie Parkinsona. W rzeczywistości, mysie modele chorób Alzheimera i Huntingtona, które są rutynowo stosowane w laboratoriach na całym świecie, nie wykazują niektórych kluczowych cech tych chorób. Na przykład neurony, które zwykle umierają u ludzi, w jakiś sposób przeżywają. Zatem model nie musi być idealny, aby był niezwykle przydatny, nawet podczas testowania potencjalnych terapii ludzkich.

Poręczny przewodnik do rozszyfrowywania psychologii myszy.

Góra: Podwyższony poziom cytokin stwierdzono w trzech różnych częściach mózgu pacjentów z autyzmem. Płaski szary prostokąt u dołu wykresu pokazuje odpowiadające poziomy w typowych mózgach. Dół: Poziomy cytokin w płynie mózgowo-rdzeniowym autystycznych (fioletowych) i niedotkniętych (żółtych) osobników.
Nasze laboratorium bada model infekcji u matki. Zarażamy ciężarną mysz grypą, dotykając jej nos pipetą zawierającą roztwór ludzkiego wirusa grypy, którą następnie wdycha. Mysz staje się letargiczna, przestaje się pielęgnować, kuli się w rogu klatki, a za kilka dni wraca do zdrowia i znów zachowuje się normalnie. W odpowiednim czasie rodzi, a my badamy młode, zarówno jako niemowlęta, jak dorosłe. Obserwujemy ich zachowanie, a następnie badamy ich patologię – jak wyglądają ich mózgi.
Jakie zachowania myszy mogą być istotne w przypadku schizofrenii lub autyzmu? Ludzie często używają tak zwanego testu otwartego pola, aby badać lęk w łagodnie stresujących warunkach. Mysz umieszczona jest w obudowie z kamerą na głowie i liniami siatki na podłodze, abyśmy mogli śledzić, gdzie porusza się zwierzę. Zwykła mysz zwykle spędza na początku dużo czasu wzdłuż krawędzi pudełka, bo boi się, że niebezpiecznie jest wyjść na środek – co oczywiście może być prawdą. Ale w końcu sprawdzi większość pudełka, zatrzymując się często w celu odchylania się na tylnych łapach i wąchania powietrza. Nasze normalne myszy, które nazywamy myszami kontrolnymi, rodzą się z matek „zainfekowanych pozornie”, którym podano sterylny roztwór soli fizjologicznej bez wirusa. Te myszy robią dokładnie to samo – na początku są nieśmiałe, ale wkrótce kroczą po całym polu.
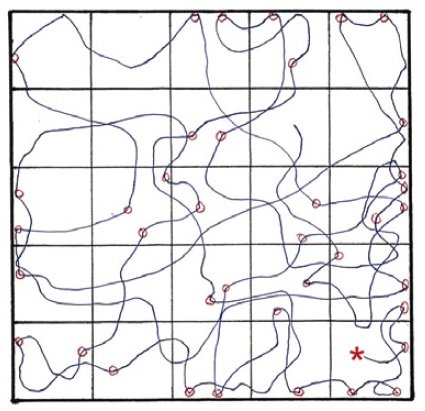
Ścieżka, po której chodzi mysz kontrolna eksplorująca nieznane miejsce. Znaki gwiazdki w miejscu, w którym mysz została umieszczona w pudełku, a czerwone kółka pokazują, gdzie mysz stała na tylnych łapach, aby uzyskać lepszy powiew otoczenia.
Poniżej znajduje się przykład dorosłej myszy, która urodziła się z matki zarażonej grypą, i można natychmiast stwierdzić na podstawie bobków kału, że wcale nie wyszła zbyt daleko od rogu. Zinterpretowalibyśmy to jako nadmiernie przerażające zachowanie, biorąc pod uwagę nieco stresujący charakter sytuacji, i możemy to określić ilościowo, po prostu mierząc czas spędzony w środkowych kwadratach pudełka. Ta mysz wchodzi do centrum pudełka o wiele rzadziej i znacznie rzadziej podnosi się na tylnych łapach i wącha.

Natomiast mysz, której matka zachorowała na grypę, skulona jest w kącie, w którym została umieszczona.
Istotny jest również tak zwany test na nowy obiekt. Pamiętaj, że dzieci autystyczne często boją się nieznanych rzeczy. Kiedy więc umieszczamy coś dziwnego i nowego w polu, powiedzmy filiżankę kawy, mysz kontrolna starannie bada to, dotykając i wąchając ze wszystkich stron, podczas gdy nasza mysz urodzona przez zarażoną [grypą] matkę bardzo niechętnie podchodzi do dowolnego miejsca w pobliżu. W rzeczywistości ta mysz odwraca głowę i zachowuje się tak, jakby nie było tam obiektu. Mierzymy upływ czasu przed pierwszym dotknięciem obiektu przez mysz, który nazywamy opóźnieniem do pierwszego kontaktu, i liczymy, jak często nawiązywane są kontakty. Znowu różnice są dramatyczne. Mysz „autystyczna” czeka znacznie dłużej i dotyka obiektu znacznie mniej razy.
Wykonujemy również proste testy interakcji społecznych. Umieszczamy dwie myszy, które się nie znają, i pytamy, ile czasu zajmuje im nawiązanie kontaktu fizycznego i jak często to robią. I nie jest to zaskakujące, że pary myszy urodzonych przez zarażone matki kontaktują się przynajmniej o połowę rzadziej oraz mają ponad czterokrotnie większe opóźnienie w nawiązaniu kontaktu. Więc najwyraźniej niewłaściwie się uspołeczniają. Teraz absolwent Steve Smith, śledzi/kontynuuje teraz tę obserwację, używając pudełka podzielonego na trzy pokoje. Umieszczamy naszą mysz testową w środkowym pokoju, a następnie umieszczamy nieznaną mysz w jednym z bocznych pomieszczeń. W niektórych testach wychodzimy z pokoju po przeciwnej pustej stronie [badanego pomieszczenia], a w innych umieszczamy w nim mysiego ziomka myszy testowej. Następnie siadamy i obserwujemy, gdzie idzie nasza mysz testowa. Normalne myszy lubią nowości i prawie zawsze podchodzą do obcej myszy, nawet gdy w drugim pokoju jest znajoma mysz. Wstępne wyniki z naszymi „autystycznymi” myszami pokazują jednak, że wolą pozostać w centralnej komnacie, niezależnie od tego, kto jeszcze jest w pudełku z nimi.

Myszy, których matki potraktowano wirusem grypy, rzadziej zapuszczały się do wielkiego pustego środka pudełka (kolumny po lewej) i spędzały tam znacznie mniej czasu (w środku). Znacznie rzadziej też podnosiły się na tylnych łapach by wąchać (po prawej).

Członek personelu działu biologii, Limin Shi, umieszcza parę myszy w trzypokojowym pudełku zaprojektowanym do testowania ich umiejętności społecznych.

U góry: Normalna mysz bada nieznany obiekt z zachłanną ciekawością. Na dole: „Autystyczna” mysz ignoruje przedmiot, najwyraźniej działając w oparciu o teorię, że jeśli nie może zobaczyć obiektu, to nie istnieje.
Kolejnym istotnym testem jest reakcja wzdrygnięcia na bodziec akustyczny, który przypomina podkradanie się za kimś z napompowaną papierową torbą i uderzenie aby pękła. Mysz umieszczamy w tubie w dźwiękoszczelnym pudełku, a pod nią znajduje się czujnik ruchu. W pudełku jest głośnik, a gdy odtwarzany jest głośny dźwięk, mysz jest zaskoczona [wzdryga się] i mierzymy, jak wysoko skacze. Ale jeśli poprzedzimy głośny dźwięk cichszym dźwiękiem, który nie przestraszy myszy – zwanym prepulsem – nie podskoczy tak bardzo. Nazywa się to testem hamowania przedsygnałowego PPI [prepulse inhibition], a gdy u ludzi wykonuje się ten sam typ testu, u pacjentów ze schizofrenią i autyzmem obserwuje się uderzający deficyt. Innymi słowy, wzdrygają się tak samo, niezależnie od tego, czy dostali impuls wstępny, czy nie. Głośny hałas zaskakuje ich za każdym razem. Uważamy, że odnosi się to do problemów z deficytem uwagi.
Na następnej stronie znajduje się wykres wartości PPI myszy w porównaniu z intensywnością impulsów przedsygnałowych. Gdy zwiększamy intensywność impulsów przedsygnałowych, uzyskujemy większe zahamowanie, ale nasze „autystyczne” myszy mają deficyt hamowania przedsygnałowego [PPI] przy każdej intensywności.
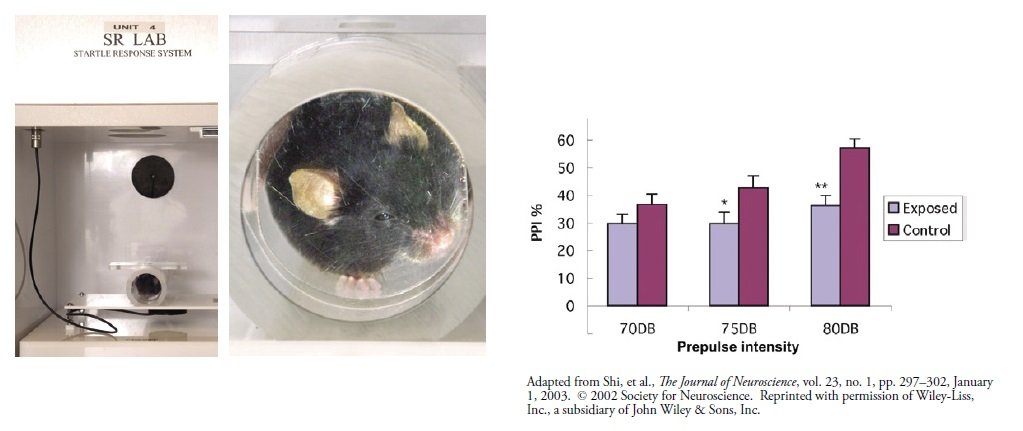
Po lewej: maszyna zaskakująca mysz. Mysz siedzi w wygodnej norce – plastikowej rurce, widocznej na tych zdjęciach, która z kolei umocowana jest na platformie z czujnikiem ruchu (czarna jednostka podłączona do czarnego kabla) na jej spodzie. Po prawej: Niezależnie od tego, jak głośny był impuls (liczby są w decybelach), mysz „autystyczna” zawsze była bardziej przestraszona – to znaczy miała mniejsze hamowanie przedsygnałowe (PPI) niż mysz kontrolna.
Uważa się, że hamowanie przedsygnałowe [PPI] jest miarą swego rodzaju tamowania czuciowo-motorycznego – połączenia między filtrowaniem przychodzących informacji sensorycznych a wytwarzaniem mocy motorycznej w mięśniach – co może być związane z deficytem uwagi i rozproszenia. W rzeczywistości deficyt hamowania przedsygnałowego PPI występuje również w zaburzeniach z niedoborem uwagi. Co ważne, wspomniane wcześniej leki przeciwpsychotyczne mogą przywrócić normalne PPI u osób schizofrenicznych, podczas gdy leki psychomimetyczne – leki halucynacyjne – zakłócają PPI. Wykazaliśmy, że to samo zjawisko ma miejsce u naszych myszy.
Zakładamy, że te nieprawidłowości behawioralne są oparte na patologii mózgu – zmianach w komórkach nerwowych lub ich połączeniach. W rzeczywistości badania pośmiertne przynajmniej niektórych mózgów pacjentów ze schizofrenią wykazały komórki nerwowe, które nie znajdują się w odpowiednich lokalizacjach. Niedawno członek personelu biologicznego Limin Shi, badacz w ramach stażu podoktoranckiego Natalia Malkova i Steve Smith przyglądali się rozwojowi mózgu płodu u myszy. Do tej analizy ciężarne myszy infekuje się grypą w połowie ciąży, w dniu 9,5 ciąży, co odpowiada okresowi bardzo wczesnego rozwoju mózgu u ludzi. Innymi słowy, jest to okres podobny do okna talidomidu z podatnością na autyzm. Jednak ponieważ myszy płodowe rozwijają się tak szybko, choroba rozciąga się także na okres odpowiadający temu drugiemu etapowi trymestru u ludzi, kiedy infekcje u matki prowadzą do zwiększonego ryzyka schizofrenii. Pięć dni po zarażeniu w myszy wstrzykuje się barwnik, który oznacza nowo utworzone neurony, i rodzą się sześć dni później. Po prawej jest mózg normalnego oseska. Zielone neurony przejęły barwnik i większość z nich wyemigrowała do tego, co neuroanatomiści nazywają warstwą 2 i 3 kory mózgowej. Jest to podobne do wyglądu normalnego nowonarodzonego ludzkiego mózgu. Ale ta warstwa jest ledwo obecna u osesków zarażonych matek. Coś poszło nie tak, ponieważ zielone komórki rozeszły się wszędzie, zamiast tworzyć normalne, ciasno upakowane warstwy. Planujemy powtórzyć eksperyment, ale pozwolimy oseskom dorosnąć, aby dojrzeć, czy ta dezorganizacja utrzymuje się i czy wygląda ona podobnie do tych, które znaleziono w kilku przykładach schizofrenii u ludzi.
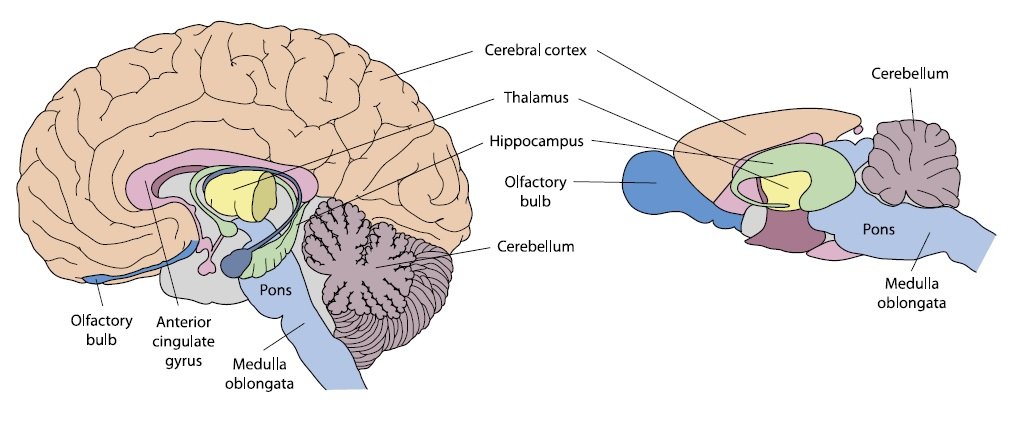
Ludzki (lewy) i myszy (prawy) mózg, obrazy nie są wykonane w skali.
Inna patologia u człowieka występuje w móżdżku. Móżdżek ma płaty zwane płacikami, które w przekroju wyglądają jak kalafior i zawierają neurony zwane komórkami Purkinjego, które występują u wszystkich gatunków ssaków. Około 90 procent pośmiertnych próbek mózgów od osób autystycznych wykazuje znaczne zmniejszenie liczby komórek Purkinjego w płacikach VI i VII. W niektórych przypadkach są nawet źle rozlokowane te komórki Purkinjego. A badania MRI żywych osobników autystycznych ujawniają, że płaciki VI i VII są niedorozwinięte.

20-miesięczne dziecko uczestniczy w bieżącym zestawie badań eksploracyjnych K. Pierce i E. Courchesne’a. Siatka na podłodze pomaga badaczom mapować ruchy dziecka. Zdjęcie dzięki uprzejmości Karen Pierce.
Istnieje fascynująca korelacja między nieprawidłowościami w płacikach VI i VII a zachowaniem eksploracyjnym dzieci. W 2001 r. Karen Pierce i Eric Courchesne z UC San Diego przeprowadzili badanie, w którym umieścili dziecko (w wieku od trzech do ośmiu lat) w pokoju z dużą ilością kolorowych pudełek i innych intrygujących przedmiotów, i policzyli, z iloma z nich dziecko bawiło się przez osiem minut. Dzieci z grupy kontrolnej średnio zbadały około 10 z 14 przedmiotów. Jednak dzieci autystyczne miały tendencję do skupiania się na kilku obiektach z wyłączeniem wszystkich innych – w jednym skrajnym przykładzie dziecko nie przeszło do kolejnych przedmiotów, po tym jak napotkało pierwszy przedmiot. Wszystkie te dzieci wcześniej miały zrobione skany MRI w ramach innego badania, i pojawiła się dramatyczna korelacja – im mniejsze płaciki VI i VII dziecka autystycznego, tym mniej obiektów zainteresowało dziecko.
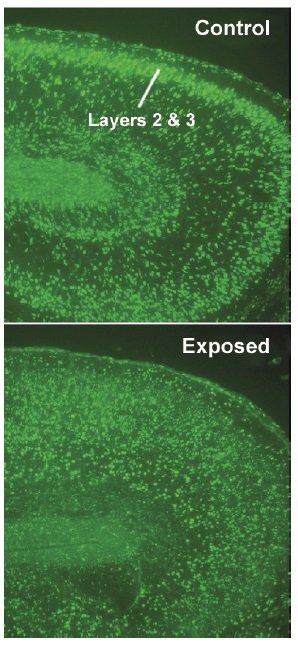
Neurony z wczesnego stadium rozwoju mózgu zostały oznaczone fluorescencyjnym zielonym barwnikiem. Te neurony tworzą wyraźnie widoczne warstwy w zdrowym nowonarodzonym mózgu myszy (u góry), ale kiedy matka została zainfekowana w czasie ciąży (u dołu), neurony są rozproszone prawie przypadkowo.
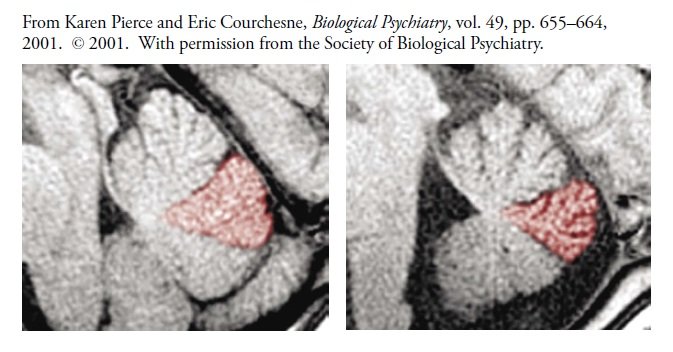
Skan MRI móżdżku kontrolnego dziecka (po lewej) i dziecka autystycznego (po prawej), z płacikami VI i VII w kolorze czerwonym
Ponieważ nasze „autystyczne” myszy były podobnie odporne na urok nieznanego obiektu, chcieliśmy sprawdzić, czy mają tę samą nieprawidłowość móżdżku. Potraktowanie móżdżku barwnikiem, który po prostu zabarwia komórki Purkinjego, ujawnia stałą różnicę u tych myszy, jak zobaczycie na następnej stronie. Ponadto od czasu do czasu widzimy, co uważamy za niewłaściwe rozlokowanie komórek Purkinjego. Komórki powinny ułożyć się w równym rzędzie wzdłuż granicy między strefą czerwoną i czarną, a nie plątać się w ciemnym wnętrzu. Uważamy, że to niewłaściwe rozlokowanie musiało wystąpić w rozwoju embrionalnym.
Teraz zastanówmy się nad mechanizmem tego, w jaki sposób działa model zwierzęcy. Czy wirus faktycznie infekuje sam mózg płodu, czy działa pośrednio przez układ odpornościowy matki? Uważamy, że to ta druga opcja, ponieważ nie możemy znaleźć wirusa u potomstwa ani w embrionalnym mózgu, ani w chwili urodzenia. Nie jest to zaskakujące, ponieważ w końcu grypa jest przede wszystkim wirusem układu oddechowego. Prawie nigdy nie wydostaje się z płuc, gardła i nosa do reszty ciała. Kiedy tak się dzieje, masz wiremię, która jest bardzo poważną chorobą.
Nano-cząsteczki metali niszczą DNA mózgu – Trinity College w Dublinie
Co więcej, możemy wywołać odpowiedź immunologiczną u matki bez użycia wirusa, po prostu przez wstrzyknięcie jej kawałka dwuniciowego RNA. Ssaki nie wytwarzają dwuniciowego RNA, ale robi to wiele wirusów, więc układ odpornościowy wie, że kiedy dostrzeże dwuniciowy RNA, musi zacząć działać. Zaczyna wydzielać cytokiny i generalnie silną reakcję przeciwwirusową, nawet jeśli nie ma infekcji. Co ciekawe, potomstwo matek, których układ odpornościowy został sztucznie aktywowany w ten sposób, wykazuje ten sam deficyt hamowania przedsygnałowego [PPI], który widzieliśmy wcześniej. Więc nie potrzebujemy wirusa; aktywacja matczynego układu odpornościowego jest wystarczająca, aby zmienić zachowanie potomstwa.

Kontrolne i „autystyczne” móżdżki myszy zabarwione barwnikiem wiążącym się z komórkami Purkinjego. Dolne dwa obrazy to zbliżenia płacika VII. Jaskrawoczerwone plamki to ciała komórek Purkinjego, a ciemne pustki są w rzeczywistości wypełnione innymi rodzajami komórek. Zdjęcie po prawej stronie – skrajny przykład, dorosłej myszy urodzonej z zainfekowanej matki – prawie nie występują komórki Purkinjego.
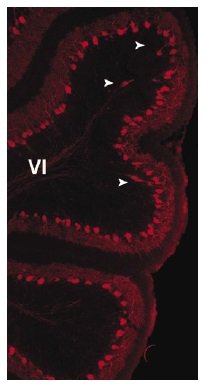
Zabłąkane komórki Purkinjego (białe groty strzałek) w środku płacika VI.
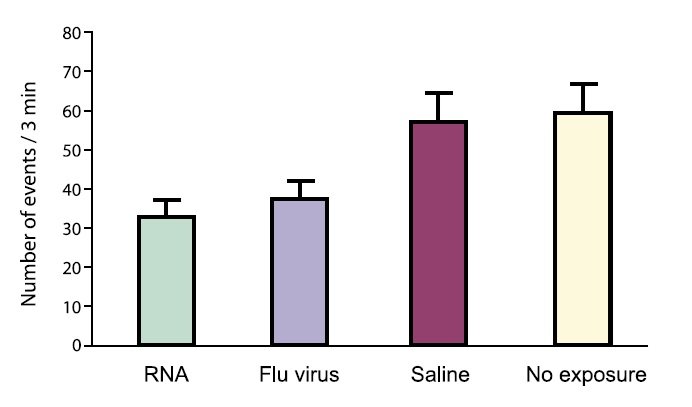
Mysie oseski urodzone przez niezainfekowane matki (żółta kolumna) płakały około 60 razy w ciągu trzech minut lub raz na trzy sekundy po oddzieleniu od mamy. Podobnie młode z grupy kontrolnej (fioletowe), których matki wdychały sterylny roztwór soli fizjologicznej. Oseski, których układ odpornościowy matek został aktywowany przez wirusa (kolor lawendy) lub kawałek dwuniciowego RNA (zielony), płakały znacznie rzadziej.
Drugi przykład zachowania „autystycznego” wywołanego przez matczyną aktywację immunologiczną odkryła Natalia Malkova. Anegdotyczne dowody sugerują, że autystyczne ludzkie dzieci mogą być mniej związane z matkami. Kiedy Natalia usuwa mysią matkę z klatki rodzinnej, zwykle powoduje znaczny płacz u osesków kontrolnych, chociaż skoro oseski myszy wokalizują na częstotliwościach ultradźwiękowych, musimy użyć specjalnego mikrofonu, aby je usłyszeć. Natalia policzyła więc, jak często młode płakały w ciągu trzech minut. Myszy urodzone przez matkę eksponowaną na podwójną nić RNA płakały mniej niż młode urodzone przez normalną matkę.
Uważamy, że aktywacja immunologiczna matki zmienia obwody mózgowe. Oprócz tego dramatycznego nieprawidłowego formowania się warstw, które Limin znajduje w korze myszy, oraz utraty komórek Purkinjego, które zaobserwowano w ludzkim móżdżku, istnieje także stały, subkliniczny, zmieniony stan odporności w autystycznym mózgu – te podwyższone poziomy cytokin. Czy te cytokiny są nieistotnym, szczątkowym śladem – skamieliną, jeśli wolisz – jakiegoś wcześniejszego zdarzenia, takiego jak infekcja matczyna? A może faktycznie wchodzą w interakcję z mózgiem w sposób ciągły, z konsekwencjami widocznymi w zachowaniu pacjentów? Popieram tę ostatnią hipotezę.
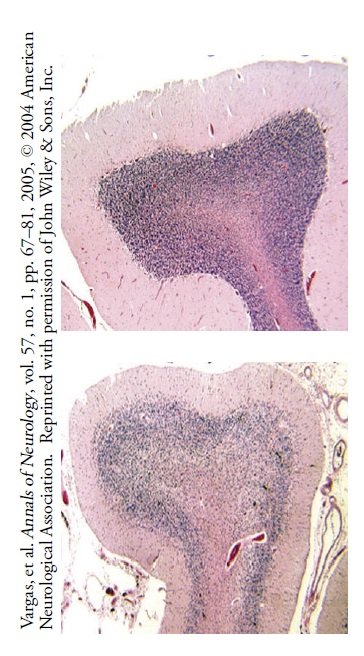
U góry: Komórki Purkinjego (fioletowoniebieskie kropki) w normalnym ludzkim móżdżku.
Na dole: Dziewięć z 10 analizowanych mózgów autystycznych wykazało nierównomierną utratę komórek Purkinjego.
W niektórych badaniach klinicznych, w których pacjenci z rakiem otrzymywali cytokiny w nadziei, że cząsteczki te zaatakują ich guzy, ujawniły się dramatyczne różnice w zachowaniu i nastroju – w najgorszym przypadku aż do ciężkiej depresji. Inni badacze stwierdzili, że wysoki poziom cytokin u zwierząt może wpływać na uczenie się i pamięć. Jeśli ta hipoteza jest prawdziwa, co by się stało, gdybyśmy zmienili stan odpornościowy mózgu? Leki przeciwpsychotyczne znane są z tłumienia układu odpornościowego. Czy ma to związek z zachowaniami psychotycznymi? Jesteśmy bardzo zainteresowani tą możliwością. W rzeczywistości Carlos Pardo z Johns Hopkins i ja organizujemy spotkanie z fundacjami Cure Autism Now i Autism Speaks w celu zbadania możliwości interwencji immunologicznej w autyzmie. Ludzie przez cały czas przyjmują leki przeciwzapalne, takie jak aspiryna, aby opóźnić odpowiedź immunologiczną – czy warto w tym kontekście zbadać tę strategię?
Właśnie zaczynamy badać interakcje między układem odpornościowym a rozwijającym się mózgiem. Cytokiny nie są jedynym możliwym kanałem od infekcji matki do rozwijającego się mózgu płodu – istnieją inne zmiany spowodowane przez kortykosteroidy, które są uwalniane po infekcji lub chorobie, które również mają wpływ na płód. I nie zapomnij o komponencie genetycznym – na jakie geny działają w celu zwiększenia podatności? Mogą bezpośrednio wpływać na rozwój mózgu płodu lub mogą wpływać na podatność mózgu na takie czynniki jak cytokiny lub odpowiedź łożyska na aktywację immunologiczną matki, a nawet mogą działać u matki, aby wpłynąć na jej odpowiedź układu odpornościowego na infekcję. Powinniśmy być w stanie ostatecznie rozwiązać te możliwości, korzystając z tego modelu zwierzęcego.
Odporność niemowląt – część 1 – Ciąża [Epigenetyka i mikrobiom]
Co to jest epigenetyka – dr Nessa Carey – Dlaczego Twoje DNA nie jest Twoim przeznaczeniem
Na koniec chcę zadać pytanie, które pojawiło się w literaturze w ciągu ostatnich kilku lat – czy naprawdę powinniśmy promować powszechne szczepienia matek? Szczepionka przeciw grypie jest rutynowo zalecana kobietom w ciąży w Stanach Zjednoczonych od 1957 roku. Oficjalna polityka Centrum Kontroli i Prewencji Chorób [CDC] stwierdza, że „podawanie szczepionek kobietom poszukującym opieki prenatalnej jest okazją do interwencji zapobiegawczej, której nie należy marnować.” Teraz możesz powiedzieć: „No cóż, oczywiście, że nie chcesz zachorować na grypę, jeśli jesteś w ciąży!”. Pamiętaj jednak o tym doświadczeniu z dwuniciowym RNA – aktywowaliśmy układ odpornościowy i spowodowało to wszystko wpływ na płód.
A co robi szczepienie? Aktywuje układ odpornościowy.
Taki jest cel szczepienia. W praktyce nie wszystkie kobiety w ciąży otrzymują szczepionki przeciw grypie i myślę, że powszechne szczepienie kobiet w ciąży może wpędzić nas w zupełnie nowy zestaw problemów. Mam zatem nadzieję, że uda się znaleźć sposób na jakąś interwencję i naprawę uszkodzeń lub regulację układu odpornościowego. Ten model myszy to doskonałe miejsce na rozpoczęcie.

Paul Patterson, profesor nauk biologicznych w Caltech i profesor badań neurobiologicznych w Keck School of Medicine w USC, uzyskał tytuł licencjata biologii w Grinnell College w Iowa w 1965 roku, a doktorat w Johns Hopkins w 1970 roku. Był profesorem neurobiologii w Harvard Medical School przed przybyciem do Caltech w 1983 roku, podążając śladami wuja, zmarłego profesora geochemii Claira Pattersona.
„Dr Peter Patterson opracował rewolucyjne podejście do badania immunologicznych i biologicznych aspektów autyzmu i zachowania zwierząt. Podczas gdy stanem rzeczy było kiedyś podejście do zachowań autystycznych u zwierząt poprzez zmiany genetyczne, Patterson podszedł do badania, opierając się na czynnikach środowiskowych.
Podejście Pattersona zakończyło się sukcesem, ponieważ odtworzyło wszystkie trzy podstawowe zachowania w autyzmie: deficyt komunikacji, deficyt interakcji społecznych i powtarzające się stereotypowe zachowania.”- Caltech neuroscience pioneer Paul H. Patterson dies
Zobacz na: 10 wczesnych oznak autyzmu. Jak rozpoznać wczesne objawy?
Typowy i nietypowy rozwój 2-miesięcznego dziecka
Typowy i nietypowy rozwój 4-miesięcznego dziecka
Typowy i nietypowy rozwój 6-miesięcznego dziecka
Zaburzenia mitochondrialne u osób z autyzmem
Środowiskowe i genetyczne przyczyny autyzmu – dr James Lyons-Weiler
Czy chińscy naukowcy odkryli brakujący fragment układanki autyzmu? – J.B. Handley
Autyzm i Szczepionki na Świecie – Kalendarze szczepień, wskaźniki występowania autyzmu i śmiertelność poniżej 5 roku życia
Synergiczne, toksyczne działanie glifosatu i aluminium – Dr Stephanie Seneff
Dieta w Zespole Psychologiczno – Jelitowym (GAPS) w leczeniu Autyzmu i Zespołu Aspergera – dr Natasha Campbell-McBride