Szczepionki bezkomórkowe przeciw krztuścowi chronią przed chorobą, ale nie blokują zakażenia i transmisji u naczelnych.
22 październik 2013
Krztusiec w Japonii – Hilary Butler
Krztusiec i Pierwotny Grzech Antygenowy.
Wiara w szybki test [na krztuśca] doprowadziła do epidemii, której nie było
Znaczenie
Krztusiec ponownie stał się istotnym problemem zdrowia publicznego od czasu, gdy obecnie stosowane szczepionki bezkomórkowe [acelularne] przeciw krztuścowi (aP) zastąpiły starsze szczepionki pełnokomórkowe (wP). W niniejszym badaniu wykazujemy, że naczelne niebędące ludźmi, zaszczepione szczepionką bezkomórkową (aP), były chronione przed ciężkimi objawami choroby, lecz nie przed zakażeniem i z łatwością przenosiły bakterie Bordetella pertussis na osobniki kontaktowe. Szczepienie szczepionką pełnokomórkową (wP) oraz przebycie wcześniejszego zakażenia prowadziły do szybszego usuwania bakterii w porównaniu z osobnikami naiwnymi immunologicznie [osobnikami bez wcześniejszego kontaktu z patogenem] oraz zaszczepionymi szczepionka bezkomórkowymi (aP). Chociaż wszystkie grupy wykazywały silne odpowiedzi przeciwciałowe, kluczowe różnice w pamięci komórek T sugerują, że szczepienie szczepionką bezkomórkową (aP), indukuje suboptymalną odpowiedź immunologiczną, która nie jest zdolna zapobiegać zakażeniu. Dane te dostarczają wiarygodnego wyjaśnienia nawrotu krztuśca i wskazują, że osiągnięcie odporności zbiorowiskowej będzie wymagało opracowania ulepszonych strategii szczepień, które zapobiegają kolonizacji i transmisji B. pertussis.
Streszczenie
Krztusiec jest wysoce zakaźną chorobą układu oddechowego wywoływaną przez bakteryjny patogen Bordetella pertussis. [Raportowana] częstość zachorowań na krztusiec w Stanach Zjednoczonych wzrasta i w 2012 roku osiągnęła najwyższy poziom od 50 lat, czyli 42.000 przypadków. Chociaż przyczyny nawrotu krztuśca nie są w pełni poznane, stawiamy hipotezę, że obecnie stosowane szczepionki acelularne [bezkomórkowe] przeciw krztuścowi (aP) nie zapobiegają kolonizacji ani transmisji bakterii.
Aby przetestować tę hipotezę, młode pawiany zaszczepiono w wieku 2, 4 i 6 miesięcy szczepionką aP lub pełnokomórkową szczepionką przeciw krztuścowi (wP), a następnie w wieku 7 miesięcy zakażono je bakterią B. pertussis. Przebieg zakażenia oceniano poprzez ilościowy pomiar kolonizacji w popłuczynach nosogardzieli oraz monitorowanie leukocytozy i objawów klinicznych.
Pawiany zaszczepione szczepionką bezkomórkową [acelularną, aP] były chronione przed ciężkimi objawami krztuśca, lecz nie przed kolonizacją; nie usuwały zakażenia szybciej niż osobniki nieszczepione i łatwo przenosiły B. pertussis na niezaszczepione osobniki kontaktowe. Szczepienie szczepionką pełnokomórkową (wP)prowadziło do szybszego usuwania bakterii w porównaniu z osobnikami naiwnymi immunologicznie [osobnikami bez wcześniejszego kontaktu z patogenem] i zaszczepionymi szczepionką bezkomórkową (aP). Dla porównania, osobniki, które wcześniej przebyły zakażenie, nie ulegały kolonizacji podczas wtórnej ekspozycji.
Chociaż wszystkie zaszczepione i wcześniej zakażone osobniki wykazywały silną odpowiedź przeciwciałową w surowicy, stwierdzono istotne różnice w odporności komórkowej. Osobniki wcześniej zakażone oraz zaszczepione wP wykazywały silną pamięć limfocytów T pomocniczych typu 17 (Th17) swoistych dla B. pertussis oraz pamięć Th1, podczas gdy szczepienie aP indukowało odpowiedź typu Th1/Th2. Obserwacja, że szczepionka aP wywołująca odpowiedź immunologiczną niezgodną z tą, która powstaje po naturalnym zakażeniu, nie zapobiega kolonizacji ani transmisji, stanowi wiarygodne wyjaśnienie nawrotu krztuśca i sugeruje, że optymalna kontrola tej choroby będzie wymagała opracowania ulepszonych szczepionek.
Krztusiec jest wysoce zakaźną, ostrą chorobą układu oddechowego wywoływaną przez bakteryjny patogen Bordetella pertussis(1, 2). Zakażenie prowadzi do szerokiego spektrum objawów klinicznych – od łagodnych objawów oddechowych po ciężką chorobę kaszlową, której towarzyszy wyraźna leukocytoza oraz charakterystyczny świszczący wdech i wymioty po napadach kaszlu(3).Od czasu zastąpienia szczepionek pełnokomórkowych szczepionkami acelularnymi w latach 90. XX wieku, krztusiec powrócił w alarmującym tempie w Stanach Zjednoczonych, mimo ogólnokrajowego poziomu wyszczepienia przekraczającego 95%(4). Przy rekordowym poziomie 42.000 zgłoszonych przypadków w 2012 roku, krztusiec jest najczęstszą chorobą możliwą do zapobiegania szczepieniami(5). Podobny nawrót obserwuje się w całym uprzemysłowionym świecie, pomimo porównywalnie wysokiego poziomu szczepień(6–9). Zaproponowano dwie główne hipotezy wyjaśniające ten nawrót:
i) obecne szczepionki acelularne (aP) są mniej skuteczne niż szczepionki pełnokomórkowe (wP), które zastąpiły, oraz
ii) odporność indukowana przez aP wygasa szybciej, niż wcześniej zakładano(10–13). Jednakże przyczyny nawrotu krztuśca nadal nie są w pełni poznane(14, 15).
Utrudnieniem w przeciwdziałaniu temu nawrotowi jest fakt, że patogeneza krztuśca oraz odporność po naturalnym zakażeniu nie zostały dobrze zbadane u ludzi, ponieważ typowy krztusiec występuje obecnie sporadycznie ze względu na wysoki poziom wyszczepienia w krajach rozwiniętych. Badania polegające na celowym zakażaniu ludzi były proponowane, lecz nigdy nie zostały przeprowadzone z powodu szeregu problemów logistycznych i etycznych, w tym ryzyka ciężkiego przebiegu choroby, braku skutecznego leczenia już rozwiniętej infekcji oraz wysoce zakaźnego charakteru krztuśca.
Chociaż do badania krztuśca stosowano różne modele na małych zwierzętach, żaden z nich nie odtwarza w sposób adekwatny choroby występującej u ludzi(16). Aby wypełnić tę lukę, niedawno opracowaliśmy model krztuśca u naczelnych niebędących ludźmi, wykorzystując pawiany (Papio anubis) i stwierdziliśmy, że przebieg choroby jest bardzo zbliżony do ciężkiej postaci klinicznej krztuśca u ludzi.
Po zakażeniu pawiany doświadczają około dwóch tygodni intensywnej kolonizacji dróg oddechowych oraz leukocytozy, której szczyt wynosi od 30.000 do 80.000 komórek/mL, co odpowiada zakresowi obserwowanemu u niemowląt chorych na krztusiec(1, 17). Ponadto u pawianów występuje napadowy kaszel, charakteryzujący się powtarzającymi się seriami od 5 do 10 kaszlnięć. Napady kaszlu utrzymują się średnio ponad dwa tygodnie, co jest krótszym okresem niż u niektórych ciężko zakażonych dzieci, u których kaszel może trwać nawet do 12 tygodni (1, 17) .
Opisaliśmy również transmisję B. pertussis drogą powietrzną z zakażonych osobników na osobniki naiwnie immunologicznie, co jest uznawane za główną drogę przenoszenia zakażenia między ludźmi(18). Ponieważ jest to jedyny model krztuśca, który odtwarza zarówno kaszel, jak i transmisję charakterystyczną dla choroby ludzkiej, uważamy, że stwarza on unikalną możliwość przetestowania naszej hipotezy, iż szczepionki bezkomórkowe (aP) nie zapobiegają kolonizacji B. pertussis, umożliwiając tym samym transmisję wśród osób zaszczepionych.
Korzystając z tego modelu, potwierdziliśmy, że podobnie jak u ludzi szczepionki acelularne (aP) zapewniają doskonałą ochronę przed ciężkim przebiegiem choroby u pawianów. Jednak szczepionki aP nie zapobiegają kolonizacji ani po bezpośrednim zakażeniu, ani po zakażeniu drogą transmisji. Co więcej, osobniki zaszczepione szczepionką bezkomórkową (aP) są zdolne do przenoszenia choroby na naiwnych immunologicznie osobników kontaktowych.
Dla porównania, zwierzęta zaszczepione szczepionką pełnokomórkową (wP) usuwały zakażenie istotnie szybciej niż osobniki zaszczepione szczepionką bezkomórkową (aP) oraz zwierzęta niezaszczepione. Stwierdziliśmy również, że szczepienie szczepionką bezkomórkową (aP) indukuje pamięć immunologiczną typu limfocytów T pomocniczych Th2 oraz Th1, podczas gdy zakażenie naturalne oraz w mniejszym stopniu szczepienie szczepionką pełnokomórkową (wP) indukują pamięć Th17 oraz Th1. Nasze wyniki sugerują, że oprócz potencjalnego wpływu obniżonej skuteczności oraz szybszego zanikania odporności indukowanej przez aP, kluczowym czynnikiem wyjaśniającym nawrót krztuśca jest niezdolność szczepionek bezkomórkowych (aP) do zapobiegania kolonizacji i transmisji [zarażania innych].
Wyniki
Szczepionki acelularne przeciw krztuścowi chronią przed objawową chorobą, lecz nie zapobiegają zakażeniu
Kilka niedawnych badań obserwacyjnych wykazało, że dzieci pierwotnie zaszczepione szczepionką bezkomórkową (aP) są bardziej narażone na rozpoznanie krztuśca niż dzieci, które otrzymały szczepionkę pełnokomórkową (wP)(19–22). Chociaż dane te sugerują, że szczepionka bezkomórkowa (aP) jest mniej skuteczna niż pełnokomórkowa (wP) w zapobieganiu kolonizacji, częstość niezdiagnozowanego nosicielstwa B. pertussis u osób zaszczepionych pozostaje nieznana.
Aby ocenić zdolność obu typów szczepionek do zapobiegania kolonizacji oraz objawom klinicznym krztuśca, pawiany szczepiono zgodnie z amerykańskim kalendarzem szczepień w wieku 2, 4 i 6 miesięcy, stosując ludzkie dawki skojarzonych szczepionek przeciw błonicy, tężcowi i krztuścowi zawierających aP lub inaktywowaną wP (Tabela 1 zawiera listę składników każdej ze szczepionek).
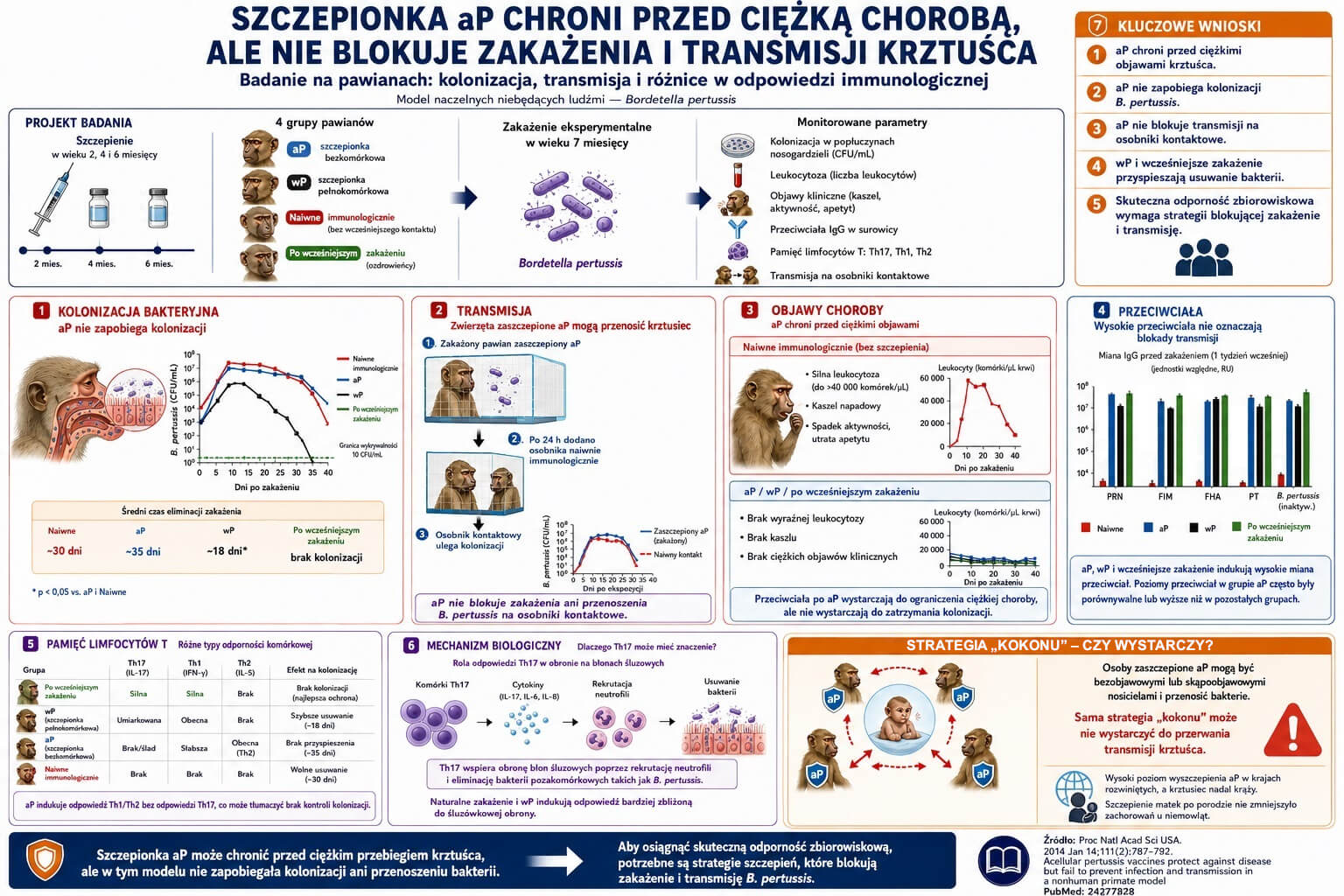
W wieku 7 miesięcy zwierzęta zaszczepione, naiwnie immunologicznie [osobniki bez wcześniejszego kontaktu z patogenem] oraz wcześniej zakażone (w fazie rekonwalescencji) poddano zakażeniu szczepem D420 – klinicznym izolatem B. pertussis powodującym ciężkie zakażenia u ludzi i pawianów(17). Zwierzęta naiwne wykazywały silną kolonizację, z poziomami szczytowymi wynoszącymi 10⁷–10⁸ jednostek tworzących kolonie na mililitr (CFU/mL) w popłuczynach nosogardzieli (Ryc. 1A). Po dwóch tygodniach kolonizacja stopniowo malała, a zakażenie ustępowało po około 30 dniach.
Zgodnie z naszymi wcześniejszymi obserwacjami, żadne ze zwierząt w fazie rekonwalescencji nie uległo kolonizacji(17). W porównaniu ze zwierzętami naiwnymi, osobniki zaszczepione szczepionką bezkomórkową (aP) wykazywały nieznacznie obniżoną kolonizację przez pierwsze 10 dni, lecz pozostawały stale skolonizowane aż do eliminacji zakażenia po 35 dniach. U zwierząt zaszczepionych szczepionką pełnokomórkową (wP) początkowy poziom kolonizacji był podobny do obserwowanego u zwierząt zaszczepionych bezkomórkową (aP), jednak zakażenie ustępowało po 18 dniach, istotnie szybciej niż u zwierząt naiwnych oraz zaszczepionych aP (Rys. 1B).
Tabela 1. Składniki szczepionek aP i wP użytych w badaniu
| Składnik szczepionki | Daptacel | Infanrix | Triple antigen |
| Toksoid błoniczy | 15 Lf | 25 Lf | 20–30 Lf |
| Toksoid tężcowy | 5 Lf | 10 Lf | 5–25 Lf |
| Pełnokomórkowa Bordetella pertussis | — | — | ≥4 IU |
| Inaktywowana toksyna krztuścowa | 10 µg | 25 µg | — |
| Hemaglutynina filamentowa | 5 µg | 25 µg | — |
| Pertaktyna | 3 µg | 8 µg | — |
| Fimbrie typu 2 i 3 | 5 µg | — | — |
| Glin (z fosforanu glinu) | 0,33 mg | ≤0,625 mg | ≤1,25 mg |
IU – jednostki międzynarodowe; Lf – jednostki granicy flokulacji (momentu, w którym cząstki w zawiesinie zaczynają się łączyć w kłaczki).
Ryc. 1. Wpływ szczepienia lub normalnego przebycia zakażenia na kolonizację i leukocytozę. Zwierzęta naiwnie immunologicznie, zaszczepione szczepionką bezkomórkową (aP), zaszczepione szczepionką pełnokomórkową (wP) oraz wcześniej zakażone (ozdrowieńcy) zostały bezpośrednio zakażone B. pertussis (n = 3–4 na grupę). (A) Kolonizację monitorowano poprzez oznaczanie liczby jednostek tworzących kolonie (cfu) B. pertussis na mL w dwutygodniowych popłuczynach nosogardzieli; granica wykrywalności wynosiła 10 cfu/mL. Dla każdego zwierzęcia czas eliminacji zakażenia zdefiniowano jako pierwszy dzień, w którym nie wykryto B. pertussis w popłuczynach nosogardzieli. (B) Przedstawiono średni czas eliminacji zakażenia dla każdej grupy (n = 3 na grupę). Ponieważ u zwierząt w fazie rekonwalescencji nie wykryto B. pertussis, średni czas eliminacji zdefiniowano jako pierwszy dzień poboru próbek (dzień 2, zaznaczony linią przerywaną). *P < 0,05 w porównaniu z grupą nieimmunizowaną (naive), †P < 0,05 w porównaniu z grupą aP, ‡P < 0,05 w porównaniu z grupą wP. (C) Przedstawiono średnią liczbę krążących białych krwinek przed zakażeniem i po zakażeniu doświadczalnym dla każdej grupy zwierząt (n = 3–4 na grupę). **P < 0,01 w porównaniu z okresem przed zakażeniem w tej samej grupie.
Aby ocenić skuteczność szczepionek w zapobieganiu objawom ciężkiego krztuśca, seryjnie pobierano krew obwodową i wykonywano pełną morfologię krwi w celu monitorowania leukocytozy, istotnego wskaźnika ciężkości choroby u niemowląt zakażonych krztuścem(23).
W porównaniu z poziomami sprzed zakażenia, u zwierząt naiwnych odnotowano istotny wzrost liczby krążących leukocytów w każdym punkcie czasowym, z maksimum przekraczającym 40 000 komórek/µL, co stanowiło ośmiokrotny wzrost względem poziomu wyjściowego (Ryc. 1C).
W przeciwieństwie do danych dotyczących kolonizacji, szczepienie szczepionką bezkomórkową (aP), szczepienie szczepionką pełnokomórkową (wP) oraz przebycie zakażenia zapobiegały leukocytozie (Ryc. 1C). Ponadto zwierzęta zaszczepione szczepionką pełnokomórkową (wP), zaszczepione szczepionką bezkomórkową (aP) oraz ozdrowieńcy nie kaszlały i nie wykazywały spadku aktywności, utraty apetytu ani innych zewnętrznych objawów choroby.
Szczepionki acelularne nie zapobiegają zakażeniu po naturalnej transmisji
Aby ocenić zdolność szczepień do zapobiegania zakażeniu krztuścem drogą transmisji, dwa zwierzęta zaszczepione szczepionką bezkomórkową (aP) oraz jedno zwierzę niezaszczepione umieszczono we wspólnej klatce z bezpośrednio zakażonym, niezaszczepionym osobnikiem.
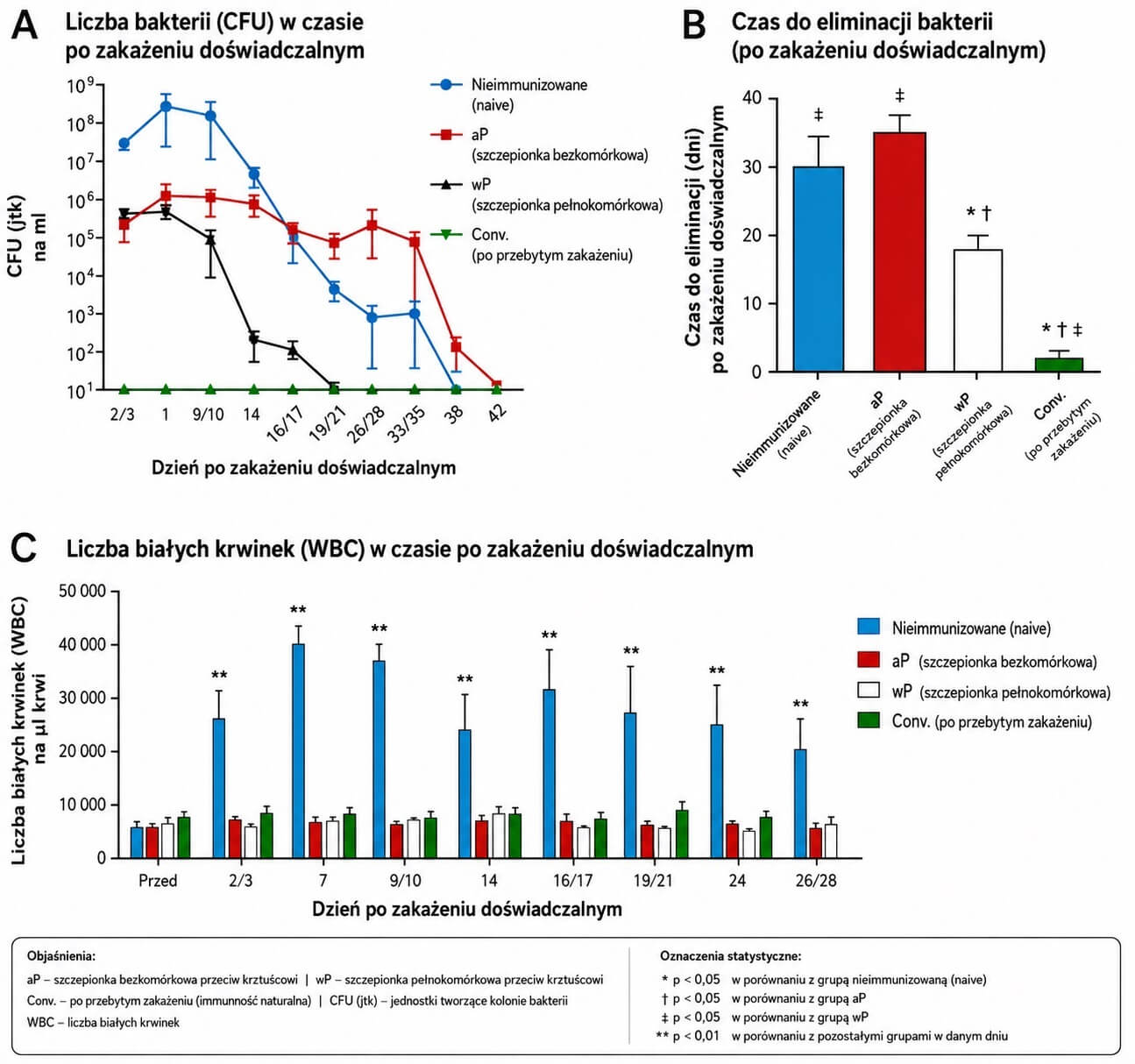
Podobnie jak w naszych wcześniejszych obserwacjach(18), wszystkie zwierzęta uległy kolonizacji po 7–10 dniach wspólnego przebywania z zakażonym osobnikiem (Ryc. 2). Szczytowe poziomy oraz dynamika kolonizacji były nie do odróżnienia między zwierzętami naiwnymi [osobnikami bez wcześniejszego kontaktu z patogenem] a zaszczepionymi szczepionką bezkomórkową (aP).
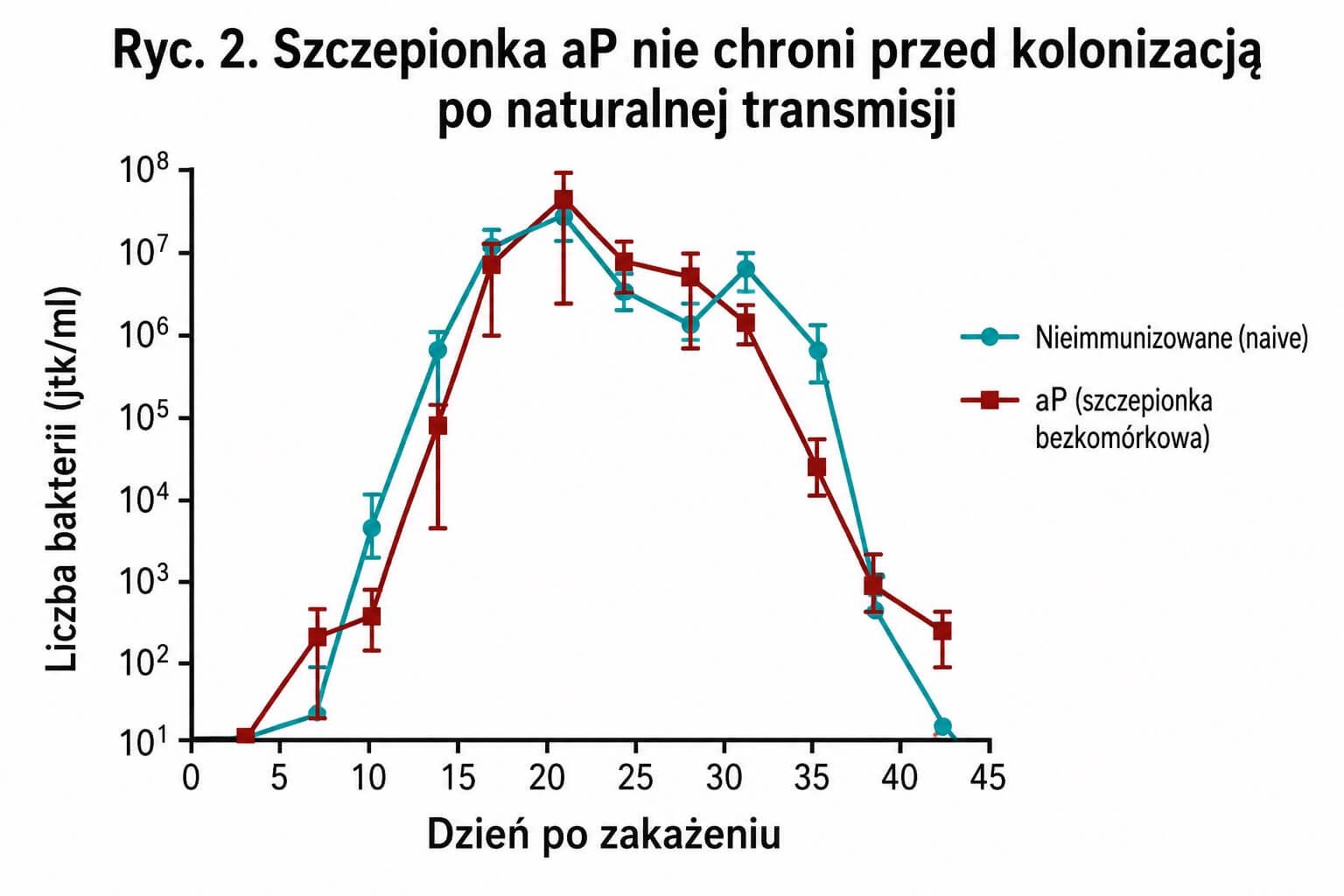
Ryc. 2. Szczepionka aP nie chroni przed kolonizacją po naturalnej transmisji. Zwierzę naiwnie immunologicznie zostało bezpośrednio zakażone. Po 24 godzinach do tej samej klatki dodano jedno zwierzę naiwnie immunologicznie oraz dwa zwierzęta zaszczepione aP i monitorowano kolonizację analogicznie jak na Ryc. 1.
Zwierzęta zaszczepione szczepionką bezkomórkową (aP) są zdolne do przenoszenia B. pertussis na osobniki bez wcześniejszego kontaktu
Ponieważ szczepionka bezkomórkowa (aP) nie zapobiega kolonizacji, postawiliśmy hipotezę, że zwierzęta zaszczepione szczepionką bezkomórkową (aP) mogą przenosić zakażenie B. pertussis na osobniki kontaktowe. Aby ją przetestować, dwa zwierzęta zaszczepione szczepionką bezkomórkową (aP) zakażono B. pertussis i umieszczono w oddzielnych klatkach. Po 24 godzinach do każdej klatki dodano jedno zwierzę naiwnie immunologicznie [bez wcześniejszego kontaktu z patogenem]i monitorowano kolonizację u wszystkich osobników.
Oba zwierzęta naiwnie immunologicznie [bez wcześniejszego kontaktu z patogenem] uległy zakażeniu w wyniku transmisji od swoich zaszczepionych szczepionką bezkomórkową (aP) współlokatorów (Ryc. 3).
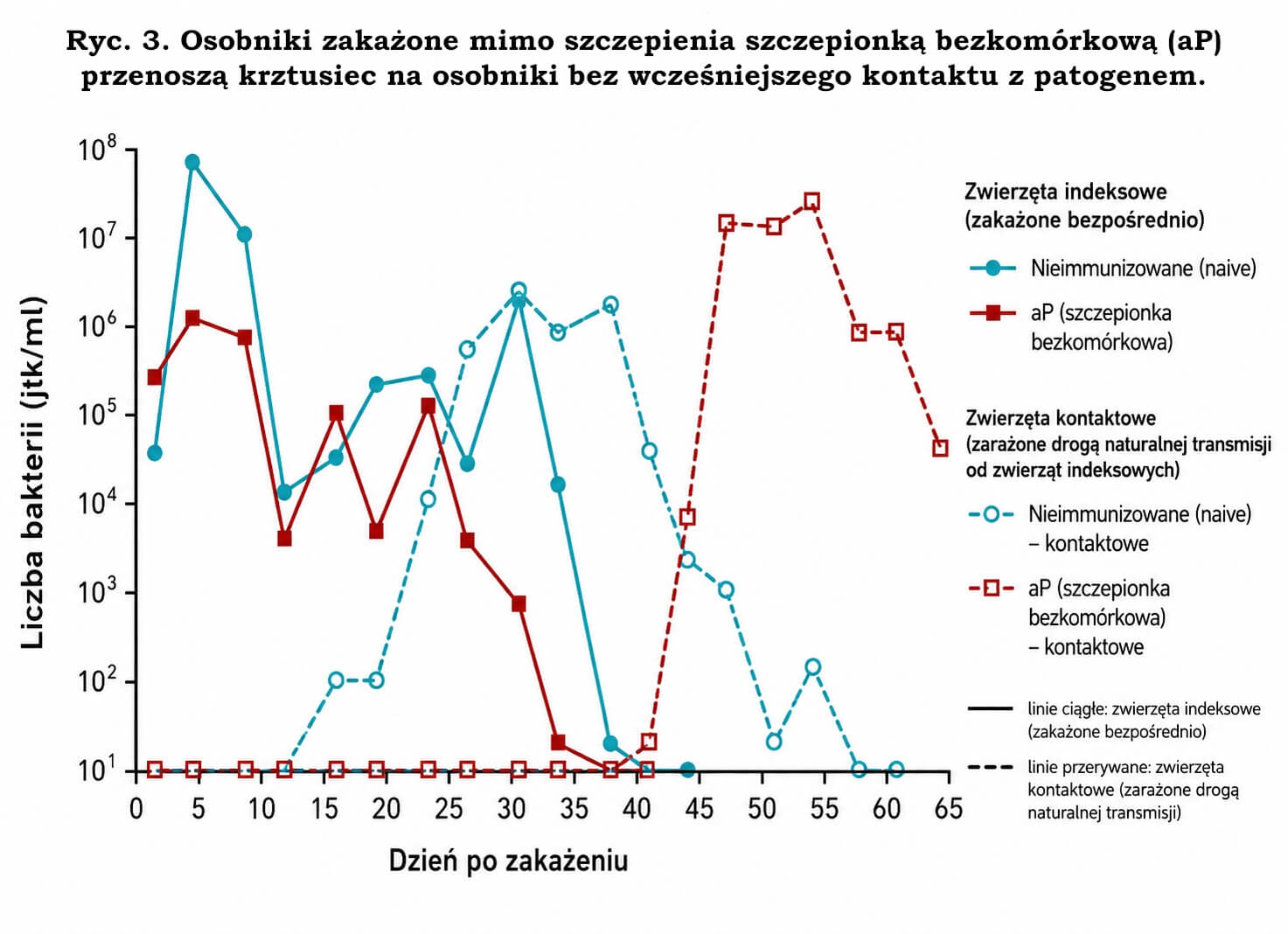
Ryc. 3. Osobniki zakażone mimo szczepienia szczepionką bezkomórkową (aP) mogą przenosić krztusiec na osobniki naiwnie immunologicznie. Dwa zwierzęta zaszczepione szczepionką aP umieszczono w oddzielnych klatkach i zakażono bezpośrednio. Po 24 godzinach do każdej klatki dodano po jednym osobniku bez wcześniejszego kontaktu z patogenem [naiwnego immunologicznie], który nie był zakażany bezpośrednio. U wszystkich zwierząt monitorowano poziom kolonizacji zgodnie z metodą opisaną na Ryc. 1. Jedną parę klatkową przedstawiono za pomocą turkusowych linii z okręgami, a drugą za pomocą bordowych linii z kwadratami. Linie ciągłe z wypełnionymi symbolami oznaczają zwierzęta zaszczepione szczepionką bezkomórkową (aP) i zakażone bezpośrednio, natomiast symbole otwarte połączone liniami przerywanymi oznaczają osobniki naiwnie immunologicznie, zakażone wyłącznie drogą naturalnej transmisji od kontaktowego zwierzęcia zakażonego.
Szczepienie i wcześniejsze zakażenie indukują silną odpowiedź przeciwciał
Surowice pobrane przed szczepieniem lub pierwotnym zakażeniem oraz ponownie na 1 tydzień przed prowokacją zakażeniem analizowano pod kątem obecności przeciwciał IgG skierowanych przeciwko zabitej termicznie B. pertussis oraz antygenom szczepionkowym: toksynie krztuścowej (PT), hemaglutyninie filamentowej (FHA), pertaktynie (PRN) oraz fimbriach typu 2 i 3 (FIM).
Wykazaliśmy, że szczepienie szczepionką pełnokomórkową (wP), szczepienie szczepionką bezkomórkową (aP) oraz naturalne zakażenie indukują wysokie miana przeciwciał wobec wszystkich antygenów, przy czym grupa szczepionki bezkomórkowej (aP) na ogół wykazywała miana przed prowokacją równoważne lub wyższe. Sugeruje to, że różnice w kolonizacji pomiędzy grupami nie korelują z poziomami krążących przeciwciał przeciwkrztuścowych (Ryc. 4).
Po prowokacji zakażeniem miana przeciwciał u zwierząt zaszczepionych pozostawały zasadniczo niezmienione, natomiast u zwierząt w fazie rekonwalescencji obserwowano wzrost (boosting) odpowiedzi wobec niektórych antygenów (Ryc. S1).
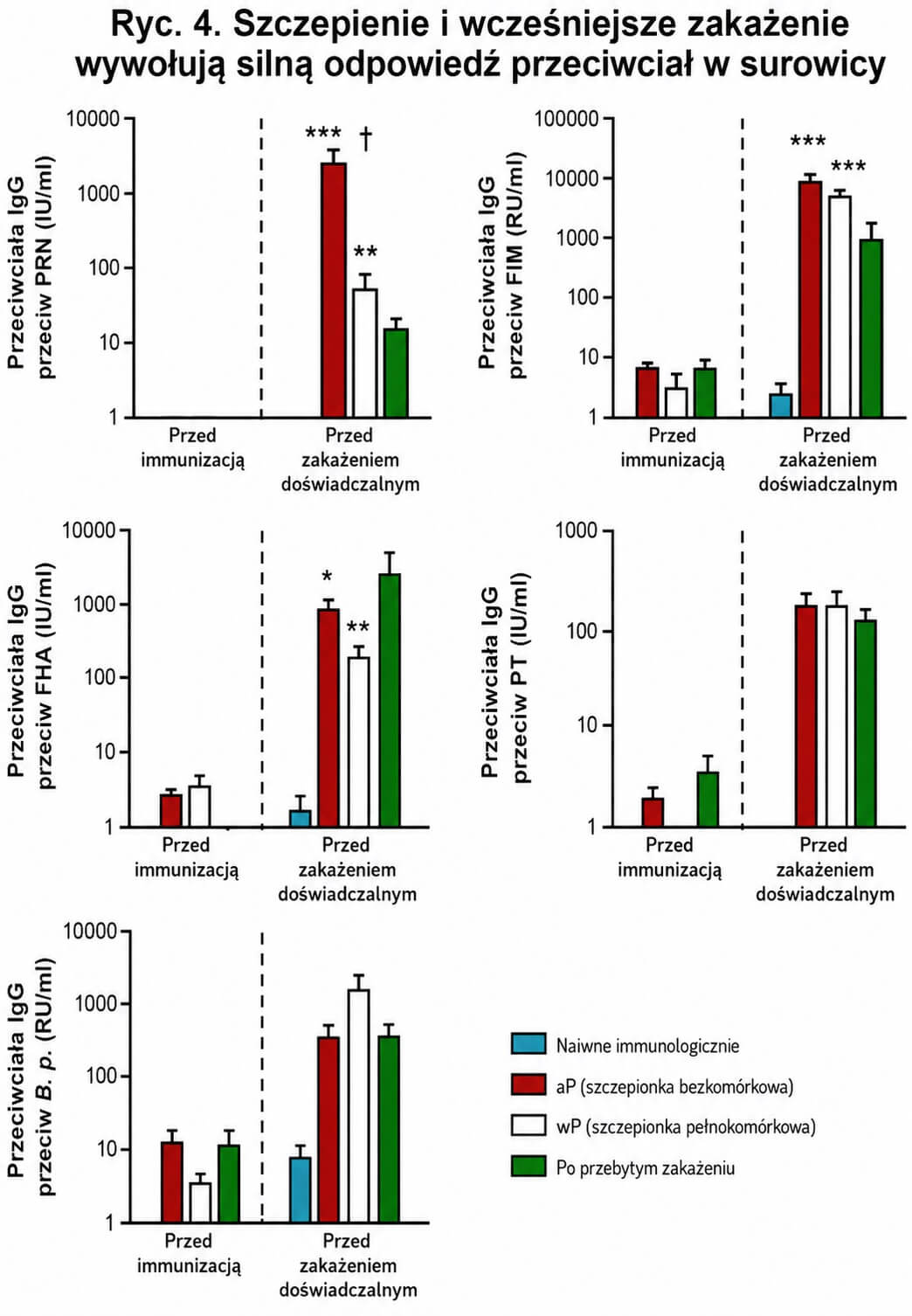
Ryc. 4. Szczepienie i wcześniejsze zakażenie wywołują silną odpowiedź przeciwciał w surowicy. Odpowiedzi przeciwciał przeciwko czterem antygenom szczepionkowym — PRN, FIM, FHA i PT — oraz przeciwko inaktywowanej cieplnie bakterii B. pertussis (B. p.) oceniano metodą ELISA. Surowicę przed immunizacją pobrano od zwierząt szczepionych przed podaniem szczepionki, a od zwierząt po przebytym zakażeniu (ozdrowieńcy) przed pierwotnym zakażeniem (n = 3–4 na grupę). Ponieważ szczepionka Infanrix nie zawiera antygenu FIM, do testu ELISA przeciw FIM włączono cztery zwierzęta zaszczepione szczepionką Daptacel. Surowicę przed zakażeniem doświadczalnym pobrano od wszystkich zwierząt tydzień przed zakażeniem. Jednostki międzynarodowe (IU) lub jednostki względne (RU) w każdej próbce określano poprzez porównanie odpowiedzi z międzynarodowym wzorcem surowicy przeciw krztuścowi WHO na każdej płytce. ***P < 0,001, **P < 0,01, *P < 0,05 w porównaniu z grupą po przebytym zakażeniu (ozdrowieńcy). †P < 0,001 w porównaniu z grupą zaszczepioną szczepionką pełnokomórkową (wP).
Pamięć odpowiedzi limfocytów T indukowana szczepieniem bezkomórkowym przeciw krztuścowi różni się od odpowiedzi po naturalnym zakażeniu.
Chociaż liczne badania kliniczne charakteryzowały odpowiedzi przeciwciał po zakażeniu krztuścem i po szczepieniu, wciąż istnieją istotne luki w naszym rozumieniu odpowiedzi immunologicznych zależnych od limfocytów T pomocniczych u ludzi i naczelnych. Co istotne, żadne badania kliniczne nie analizowały, czy podstawowy cykl szczepień przeciw krztuścowi indukuje pamięć Th17, niedawno opisaną populację limfocytów T wyspecjalizowaną w kontroli pozakomórkowych zakażeń bakteryjnych na powierzchniach śluzówkowych poprzez stymulację rekrutacji neutrofili(24).
Aby ocenić swoistą wobec B. pertussis pamięć limfocytów T u zwierząt naiwnych, zaszczepionych aP, zaszczepionych wP oraz rekonwalescentów [ozdrowieńców], na 1 tydzień przed zakażeniem pobrano jednojądrzaste komórki krwi obwodowej (PBMC). Całkowite PBMC inkubowano albo z samym podłożem, albo z zabitą termicznie B. pertussis jako symulacją ex vivo odpowiedzi pamięci, które miały zostać odtworzone podczas późniejszej prowokacji.
Po inkubacji trwającej noc wyizolowano nieadhezyjne PBMC, w tym limfocyty T, i rozdzielono je przy użyciu kulek magnetycznych na następujące frakcje: CD4−, CD4+, CD95–CD4+ lub pozostawiono nierozdzielone (całkowite komórki nieadhezyjne). U naczelnych pamięciowe limfocyty T pomocnicze charakteryzują się ekspresją powierzchniową CD4 i CD95(25, 26).
Po dalszej hodowli wszystkich frakcji analizowano supernatanty pod kątem wydzielania IL-17, IFN-γ oraz IL-5 — cytokin charakterystycznych odpowiednio dla komórek Th17, Th1 i Th2. Bardzo niskie wydzielanie cytokin w tle obserwowano w komórkach niestymulowanych, izolowanych od zwierząt naiwnych, zaszczepionych i rekonwalescentów oraz w komórkach stymulowanych pochodzących od zwierząt naiwnych (Ryc. S2 i S3).
Po stymulacji zabitą termicznie B. pertussis zarówno całkowite komórki nieadhezyjne, jak i komórki CD4+ pochodzące od rekonwalescentów wydzielały wysokie poziomy IL-17, pewne ilości IFN-γ oraz brak IL-5. Po usunięciu komórek pamięci CD95+, komórki CD95–CD4+ nie wydzielały IL-17 ani IFN-γ, co jest zgodne z indukcją swoistej wobec B. pertussis pamięci Th17 i Th1 (Ryc. 5).
Stymulowane całkowite komórki nieadhezyjne oraz komórki CD4+ pochodzące od zwierząt zaszczepionych aP wydzielały istotne ilości IFN-γ, jednak odpowiedź ta była słabsza niż u rekonwalescentów (P = 0,01), a nie obserwowano istotnego wzrostu wydzielania IL-17. Natomiast zaobserwowano istotną odpowiedź IL-5, co wskazuje na przesunięcie odpowiedzi w kierunku pamięci Th2 i Th1 (Ryc. 5).
Całkowite komórki nieadhezyjne oraz komórki CD4+ od zwierząt zaszczepionych szczepionką pełnokomórkową (wP) wydzielały podobne ilości IFN-γ jak komórki z grupy zaszczepionej szczepionką bezkomórkową (aP), ale nie wydzielały IL-5. Wydzielanie IL-17 było pośrednie między poziomami obserwowanymi u zwierząt naiwnych i rekonwalescentów, co sugeruje, że pamięć limfocytów T indukowana przez szczepionkę pełnokomórkową (wP) jest bardziej zbliżona do tej po naturalnym zakażeniu, choć odpowiedzi Th17 i Th1 są słabsze.
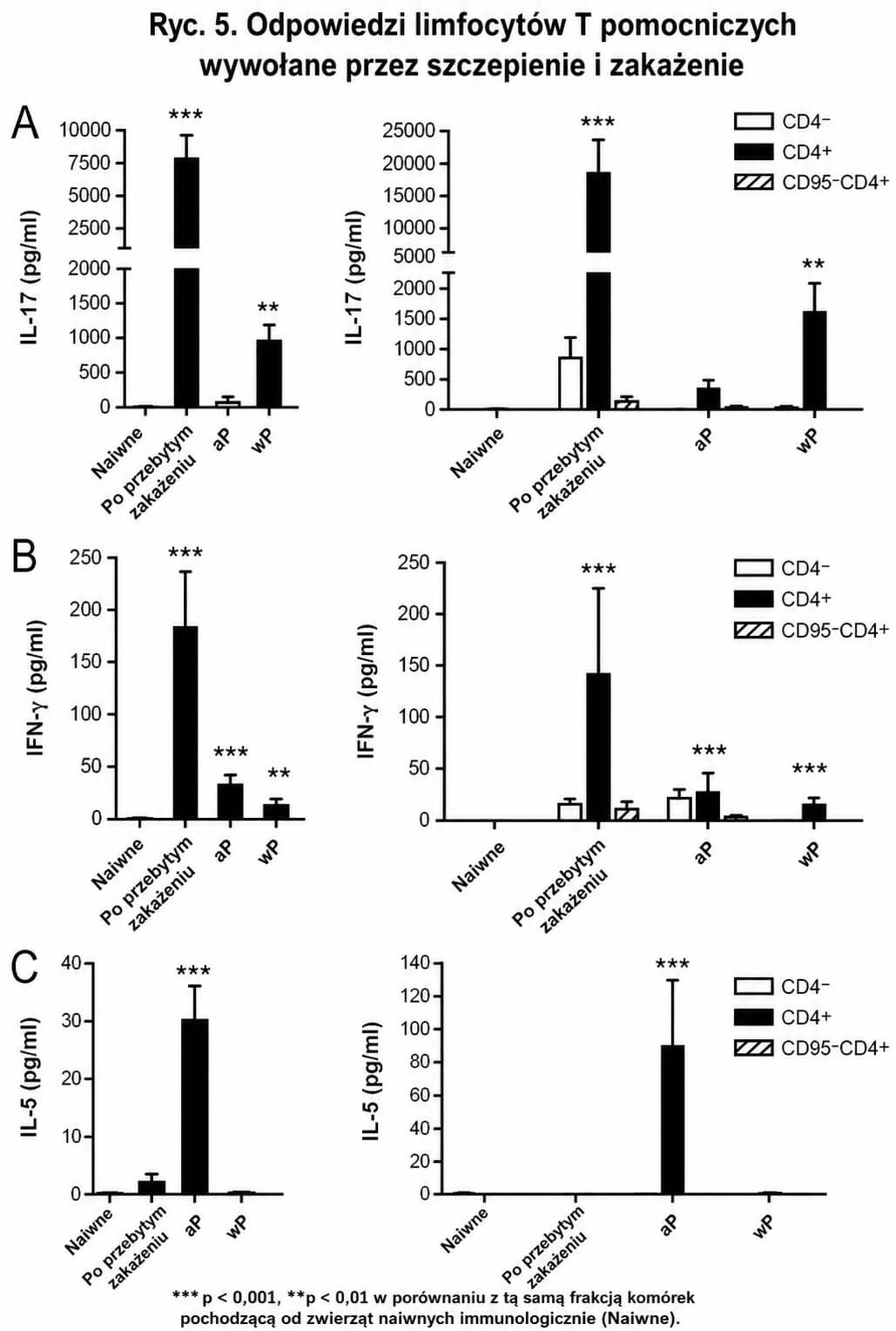
Ryc. 5. Odpowiedzi limfocytów T pomocniczych wywołane przez szczepienie i zakażenie. Komórki PBMC pobrane od zwierząt naiwnych immunologicznie, zaszczepionych szczepionką aP, zaszczepionych szczepionką wP oraz po przebytym zakażeniu (ozdrowieńcy) na tydzień przed zakażeniem inkubowano przez noc albo w samym podłożu hodowlanym, albo w podłożu zawierającym inaktywowaną cieplnie bakterię B. pertussis (n = 3–4 na grupę). Dla każdego wariantu hodowli komórki nieadherentne zostały zebrane i albo pozostawione bez rozdzielania (całkowita populacja komórek nieadherentnych), albo rozdzielone za pomocą magnetycznych cząstek przeciw CD4 i CD95. Następnie całkowite komórki nieadherentne, komórki CD4−, CD4+ oraz CD95−CD4+ hodowano w tych samych warunkach co wcześniej (w samym podłożu lub po stymulacji inaktywowaną cieplnie bakterią B. pertussis). Po 36 godzinach zebrano supernatanty i oznaczono poziomy IL-17 (A), IFN-γ (B) oraz IL-5 (C). Wydzielanie cytokin w odpowiedzi na stymulację B. pertussis przedstawiono dla całkowitej populacji komórek nieadherentnych (po lewej) oraz dla rozdzielonych populacji komórkowych (po prawej). ***P < 0,001, **P < 0,01, *P < 0,05 w porównaniu z odpowiadającą frakcją komórek pochodzącą od zwierząt naiwnych immunologicznie.
Dyskusja
Wprowadzenie w Stanach Zjednoczonych w latach 40. XX wieku szczepionek pełnokomórkowych, składających się z inaktywowanych bakterii Bordetella pertussis, spowodowało gwałtowny spadek zachorowań na krztusiec(27). Jednak w ciągu ostatnich 30 lat krztusiec ponownie się nasilił w USA. Wzrost zachorowań rozpoczął się jeszcze w okresie stosowania szczepionek pełnokomórkowych (wP), ale jego tempo wyraźnie przyspieszyło po wprowadzeniu zaleceń stosowania szczepionek bezkomórkowych (aP) we wszystkich dawkach podstawowych i przypominających(11).
Ta korelacja doprowadziła wielu badaczy do hipotezy, że szczepionki bezkomórkowe (aP) są na poziomie populacyjnym mniej skuteczne niż szczepionki pełnokomórkowe (wP), które zastąpiły(10, 12, 13). Zgodnie z tym poglądem kilka niedawnych badań obserwacyjnych wykazało, że dzieci szczepione pierwotnie szczepionką aP miały od dwukrotnie do pięciokrotnie wyższe ryzyko rozpoznania krztuśca w porównaniu z dziećmi szczepionymi wP(19–22).
Nasze wyniki uzyskane u naczelnych innych niż człowiek stanowią rozszerzenie tych obserwacji, pokazując, że zwierzęta zaszczepione szczepionką pełnokomórkową (wP) eliminowały zakażenie po bezpośrednim zakażeniu dwukrotnie szybciej niż zwierzęta zaszczepione szczepionką bezkomórkową (aP). Jednak żadna ze szczepionek nie była w stanie zapobiegać kolonizacji tak skutecznie, jak odporność nabyta po wcześniejszym zakażeniu.
Inna hipoteza tłumacząca ponowny wzrost zachorowań na krztusiec zakłada, że czas trwania odporności u dzieci zaszczepionych aP jest krótszy, niż pierwotnie przewidywano. Chociaż niektóre szczepionki bezkomórkowe [acelularne] pierwszej generacji charakteryzowały się słabą immunogennością i skutecznością, randomizowane, podwójnie zaślepione badania kliniczne oraz badania skuteczności terenowej dla dopuszczonych w USA szczepionek aP wykazywały bardzo wysoką skuteczność krótkoterminową: około 85% po trzech dawkach oraz 98% po pięciu dawkach(28–30).
Jednak niedawne badania kohortowe oraz badania kliniczno-kontrolne wykazały, że po upływie 5 lat od podania piątej dawki szczepionki bezkomórkowej (aP) dzieci są od czterech do piętnastu razy bardziej narażone na zachorowanie na krztusiec niż w ciągu pierwszego roku po szczepieniu, co jest zgodne ze stopniowym wygasaniem odporności indukowanej przez szczepionkę aP(30–33).
Postawiliśmy hipotezę, że dodatkowym wyjaśnieniem nawrotu krztuśca może być fakt, iż osoby zaszczepione szczepionką bezkomórkową (aP) mogą działać jako bezobjawowi lub skąpoobjawowi nosiciele i w istotny sposób przyczyniać się do transmisji zakażenia w populacji. Badania obserwacyjne sugerują, że bezobjawowy krztusiec może występować zarówno u zaszczepionych dzieci, jak i dorosłych, co wykazano na podstawie danych PCR oraz badań serologicznych(34, 35).
Jednak podczas badań klinicznych nad szczepionką bezkomórkową (aP) uczestnicy nie byli badani w kierunku zakażenia Bordetella pertussis, chyba że występowały u nich objawy przypominające krztusiec oraz kaszel utrzymujący się przez co najmniej 7–21 dni(12). W związku z tym nie istnieją eksperymentalne dane dotyczące tego, czy szczepienie zapobiega kolonizacji lub transmisji B. pertussis u ludzi.
W niniejszym badaniu wykazaliśmy, że naczelne zaszczepione szczepionką bezkomórkową (aP) były silnie zakażone po bezpośrednim zakażeniu eksperymentalnym, a czas eliminacji bakterii nie różnił się od obserwowanego u zwierząt naiwnych immunologicznie. Podobnie nie stwierdzono różnic ani w dynamice kolonizacji, ani w szczytowym poziomie kolonizacji pomiędzy zwierzętami zaszczepionymi aP a zwierzętami naiwnymi zakażonymi drogą naturalnej transmisji.
Co istotne, w dwóch eksperymentach wykazaliśmy również, że zwierzęta zaszczepione szczepionką aP przenosiły Bordetella pertussis na naiwnych współlokatorów klatkowych. Łącznie dane te prowadzą do kluczowego wniosku tego badania: szczepionki bezkomórkowe przeciw krztuścowi (aP) nie zapobiegają zakażeniu ani transmisji Bordetella pertussis nawet miesiąc po zakończeniu podstawowego schematu szczepienia.
Wykazaliśmy, że szczepionki pełnokomórkowe (wP), bezkomórkowe (aP) oraz naturalne zakażenie indukują wysokie miana przeciwciał. Miana przeciwciał przed zakażeniem eksperymentalnym u zwierząt zaszczepionych szczepionką aP były na ogół porównywalne lub wyższe niż obserwowane u zwierząt po przebytym zakażeniu oraz zaszczepionych szczepionką wP, co sugeruje, że szczepionka aP jest immunogenna u pawianów, a brak zdolności do zapobiegania zakażeniu nie wynikał z niskiego poziomu przeciwciał.
W porównaniu z dużą liczbą badań klinicznych charakteryzujących odpowiedź przeciwciał po zakażeniu krztuścem i szczepieniu, bardzo niewiele badań analizowało odpowiedzi immunologiczne limfocytów T pomocniczych indukowane przez krztusiec u ludzi. Łącznie te ograniczone dane sugerują, że szczepienie szczepionką aP wywołuje odpowiedź typu Th2 lub mieszaną odpowiedź Th2/Th1, podczas gdy szczepienie szczepionką wP oraz naturalne zakażenie indukują odpowiedź typu Th1(13).
Jednak żadne z tych badań nie analizowało pamięci immunologicznej Th17, stosunkowo niedawno zidentyfikowanej populacji limfocytów T wyspecjalizowanych w kontrolowaniu zewnątrzkomórkowych zakażeń bakteryjnych na powierzchniach błon śluzowych(24). Nasze dane pokazują, że naturalne zakażenie indukowało silną odpowiedź immunologiczną typu Th17 oraz Th1. Zwierzęta zaszczepione szczepionką pełnokomórkową (wP), które eliminowały zakażenie szybciej niż zwierzęta naiwne oraz zaszczepione szczepionką aP, wykazywały podobne, lecz słabsze odpowiedzi limfocytów T.
Powszechnie uważa się, że szczepionki wP indukują silną odpowiedź Th1, jednak obserwowana przez nas odpowiedź była stosunkowo słaba. Obserwację tę można tłumaczyć różnicami w procesie produkcji różnych szczepionek wP. Przyszłe badania będą porównywać odpowiedzi immunologiczne indukowane przez szczepionki wP pochodzące od trzech różnych producentów.
W porównaniu z naturalnym zakażeniem oraz szczepionką wP, odporność indukowana przez szczepionkę aP była niedopasowana, dominowała odpowiedź typu Th2, z osłabioną odpowiedzią Th1 oraz brakiem istotnej odpowiedzi Th17.
Łącznie dane dotyczące cytokin oraz odpowiedzi immunologicznych limfocytów T obserwowane u pawianów są zasadniczo zgodne z wynikami uzyskanymi wcześniej u myszy(13). Wcześniej wykazaliśmy, że zakażenie krztuścem u pawianów indukuje odpowiedź immunologiczną błon śluzowych charakteryzującą się produkcją IL-17 oraz szeregu chemokin i cytokin związanych z sygnalizacją IL-17, w tym IL-6 i IL-8. Ta pierwotna odpowiedź immunologiczna korelowała z długotrwałą pamięcią immunologiczną typu Th17 i Th1 utrzymującą się przez ponad 2 lata(36).
Myszy zakażone Bordetella pertussis również wykazują ekspresję śluzówkowych homologów IL-17, IL-6 i IL-8 oraz rozwijają pamięć immunologiczną typu Th17 i Th1(37–40). Myszy szczepione szczepionką pełnokomórkową (wP) także rozwijają pamięć Th17 i Th1, która prowadzi do częściowej odporności ochronnej, podobnie jak obserwowaliśmy to w modelu pawiana(41, 42).
Niedawny raport Ross i wsp.(42) wykazał, że szczepionka bezkomórkowa (aP) zawierająca PT, FHA i PRN indukuje odpowiedzi immunologiczne typu Th1, Th2 oraz Th17 u myszy C57BL/6 (42). Jednak wcześniejsze badanie tej samej grupy wykazało odpowiedzi Th1 i Th2, ale brak istotnej odpowiedzi Th17 u szczepów myszy C3H/HeJ oraz C3H/HeN szczepionych preparatem aP zawierającym PT i FHA(41).
Niemniej jednak dane z dwóch badań klinicznych przeprowadzonych ostatnio wykazały znikome odpowiedzi pamięciowe Th17 (około 10 pg/ml) w komórkach PBMC izolowanych od czteroletnich dzieci zaszczepionych szczepionką aP, zarówno przed dawką przypominającą, jak i po niej. Wyniki te sugerują, że szczepionki aP nie indukują pamięci immunologicznej Th17 u ludzi(43, 44).
Łącznie dane przedstawione w tym badaniu sugerują, że przeciwciała indukowane przez szczepienie szczepionką bezkomórkową (aP) są wystarczające do zapobiegania ciężkim objawom krztuśca, jednak nie ograniczają kolonizacji bakterii. Hamowanie leukocytozy prawdopodobnie zachodzi poprzez neutralizację toksyny krztuścowej (PT) za pośrednictwem przeciwciał. Toksyna ta zaburza przenikanie leukocytów z naczyń do tkanek poprzez blokowanie sygnalizacji receptorów chemokinowych(1).
Mechanizm, dzięki któremu szczepionka aP zapobiega kaszlowi pomimo znacznej kolonizacji bakteryjnej, nie jest obecnie znany, jednak wymaga dalszych badań.
Z drugiej strony indukcja pamięci immunologicznej typu Th17/Th1 korelowała ze zdolnością do eliminacji zakażenia: zwierzęta po przebytym zakażeniu oraz zaszczepione szczepionką pełnokomórkową (wP) wykazywały silne odpowiedzi Th17 i Th1 oraz eliminowały zakażenie szybciej niż zwierzęta zaszczepione szczepionką aP, które nie wykazywały odpowiedzi Th17, lecz posiadały pamięć immunologiczną typu Th1/Th2.
Chociaż nie wykazaliśmy jednoznacznie, że komórki Th17 są niezbędne do eliminacji Bordetella pertussis, obserwowana korelacja jest zgodna z rolą tych komórek w zwalczaniu zewnątrzkomórkowych zakażeń bakteryjnych na powierzchniach błon śluzowych poprzez indukowanie chemotaksji neutrofili.
Obecne badania nie były projektowane pod kątem analizy rekrutacji komórek odpornościowych do dróg oddechowych, jednak prowadzone są dodatkowe eksperymenty mające określić rolę neutrofili w odpowiedzi immunologicznej na zakażenie krztuścem i szczepienie u pawianów.
Badamy również inne możliwe mechanizmy mogące zapobiegać kolonizacji błon śluzowych, między innymi potencjalną rolę przeciwciał IgA oraz IgD, które są wydzielane odpowiednio w dolnych i górnych drogach oddechowych naczelnych(45, 46).
Model pawiana oferuje wiele zalet, przede wszystkim możliwość badania patogenezy krztuśca, transmisji zakażenia oraz odpowiedzi immunologicznej gospodarza na infekcję i szczepienie u gatunku naczelnych, który jest w ponad 96% genetycznie podobny do człowieka(47). Model ten ma jednak również istotne ograniczenia. Przede wszystkim dostępnych jest znacznie mniej zwierząt do badań niż w przypadku modeli opartych na mniejszych gatunkach. Ponadto istnieje niedobór odczynników immunologicznych zwalidowanych dla pawianów w porównaniu z myszami i ludźmi.
Chociaż przeciwciała skierowane przeciwko markerom powierzchniowym komórek są zazwyczaj reaktywne krzyżowo, przeciwciała antycytokinowe są znacznie bardziej swoiste gatunkowo. Z tego powodu do tej pory nie byliśmy w stanie ocenić odpowiedzi limfocytów T za pomocą barwienia cytokin wewnątrzkomórkowych i cytometrii przepływowej. Skłoniło nas to do opracowania testu separacji komórek jako alternatywnej metody fenotypowania odpowiedzi pamięci limfocytów T indukowanych przez zakażenie krztuścem i szczepienie(36).
Jednym z ograniczeń naszego testu jest to, że podczas oczyszczania komórek CD4⁺ usuwane są komórki prezentujące antygen, takie jak makrofagi i komórki dendrytyczne, po całonocnej inkubacji. Prawdopodobnie wyjaśnia to niski poziom wydzielania IFN-γ obserwowany we wszystkich grupach, ponieważ komórki prezentujące antygen zwiększają wydzielanie IFN-γ przez swoiste antygenowo limfocyty T CD4⁺ poprzez dodatnią pętlę sprzężenia zwrotnego(48).
Zgodnie z tą hipotezą nasze wcześniejsze dane wykazały, że ponownie stymulowane całe PBMC pochodzące od zwierząt po przebytym zakażeniu wydzielały znacznie wyższe poziomy IFN-γ. Ponadto testy restymulacyjne wykorzystujące ludzkie PBMC lub splenocyty mysie po zakażeniu albo szczepieniu również wykazują wyższe poziomy wydzielanego IFN-γ(42, 49).
Łącznie obserwacje te sugerują, że chociaż nasz test jest wartościowy do fenotypowania pamięci limfocytów T, prawdopodobnie nie doszacowuje wielkości odpowiedzi pamięciowej typu Th1.
W naszych testach restymulacyjnych wykorzystaliśmy zabite termicznie Bordetella pertussis jako antygen, ponieważ uważamy, że jest to najbardziej adekwatna metoda symulacji ex vivo pamięci limfocytów T aktywowanej podczas zakażenia. Możliwe jednak, że taki test nie wykrywa części odpowiedzi immunologicznych, które byłyby obserwowane przy użyciu oczyszczonych antygenów szczepionkowych.
Kolejną wadą modeli naczelnych jest brak możliwości bezpośredniego powiązania konkretnej odpowiedzi immunologicznej z poziomem ochrony. Chociaż wykazano, że ochrona przed krztuścem jest zależna od IFN-γ oraz — w mniejszym stopniu — od sygnalizacji IL-17 przy użyciu szczepów myszy knockout pozbawionych określonych produktów genowych(13), względny poziom ochrony zapewniany przez odpowiedzi typu Th17 lub Th1 u zaszczepionych lub rekonwalescencyjnych pawianów oraz ludzi pozostaje nieznany.
Obecnie jednym z głównych celów instytucji zdrowia publicznego jest zapobieganie zakażeniom krztuścem u małych niemowląt, które nie zakończyły jeszcze podstawowego cyklu szczepienia szczepionką bezkomórkową (aP) i są szczególnie narażone na ciężki przebieg choroby oraz wysoką śmiertelność związaną z zakażeniem krztuścem(1).
Jednym z zalecanych sposobów ograniczenia transmisji krztuśca na niemowlęta jest strategia „kokonu” (cocooning), polegająca na szczepieniu osób mających kontakt z niemowlętami(11).
Nasze dane pokazują jednak, że zwierzęta zaszczepione szczepionką aP mogą ulegać zakażeniu i przenosić krztusiec na naiwne immunologicznie osobniki. Zgodnie z tymi obserwacjami badania seroepidemiologiczne wykazały, że krążenie Bordetella pertussis pozostaje wysokie nawet w krajach o bardzo wysokim poziomie wyszczepienia szczepionką aP(27, 50), a badanie przekrojowe wykazało, że szczepienie matek szczepionką aP po porodzie nie zmniejszało liczby zachorowań na krztusiec u małych niemowląt(51). Dane te sugerują, że strategia „kokonu” prawdopodobnie nie jest skuteczną metodą zmniejszania obciążenia krztuścem u niemowląt.
Jednocześnie należy podkreślić, że nasze dane, w połączeniu z wynikami badań u ludzi, pokazują, iż szczepienie szczepionką aP zapewnia bardzo dobrą ochronę przed ciężkim przebiegiem krztuśca(52). Dlatego wszelkie krótkoterminowe działania mające przeciwdziałać nawrotowi krztuśca powinny obejmować dalsze wysiłki na rzecz utrzymania i poprawy szczepień szczepionką aP.
Jednak aby skutecznie chronić najbardziej narażonych członków populacji oraz osiągnąć optymalną odporność zbiorowiskową, konieczne będzie opracowanie strategii szczepień, która skutecznie blokowałaby zarówno zakażenie, jak i transmisję krztuśca.
Źródło: Proc Natl Acad Sci USA. 2014 Jan 14;111(2):787-92; Acellular pertussis vaccines protect against disease but fail to prevent infection and transmission in a nonhuman primate model https://pubmed.ncbi.nlm.nih.gov/24277828/
Zobacz na: Arystoteles: Ojciec Logiki – Historia Filozofii Zachodniej (część 15 z 50)
Krztusiec wśród całkowicie zaszczepionych dzieci w ośrodkach opieki dziennej w Izraelu [2000]
Zeznania dr Stanley’a Plotkina pod przysięgą – cz. 3, krztusiec, szczepienie w ciąży, konflikty interesów

Bibliografia:
1. S. Mattoo, J.D. Cherry, Molecular pathogenesis, epidemiology, and clinical manifestations of respiratory infections due to Bordetella pertussis and other Bordetella subspecies. Clin Microbiol Rev 18, 326–382 (2005).
U. Heininger, Update on pertussis in children. Expert Rev Anti Infect Ther 8, 163–173 (2010).
J.D. Cherry, U. Heininger, Pertussis and other Bordetella infections. W: Textbook of Pediatric Infectious Diseases, red. R.D. Feigin, J.D. Cherry, G.J. Demmler-Harrison, S.L. Kaplan (W.B. Saunders, Philadelphia), s. 1683–1706 (2009).
Centers for Disease Control and Prevention (CDC), National, state, and local area vaccination coverage among children aged 19–35 months—United States, 2011. MMWR Morb Mortal Wkly Rep 61, 689–696 (2012).
CDC, Notifiable diseases and mortality tables. MMWR Morb Mortal Wkly Rep 61, ND-719–ND-732 (2012).
D. Hozbor i in., Pertussis epidemiology in Argentina: Trends over 2004–2007. J Infect 59, 225–231 (2009).
H.E. Quinn, P.B. McIntyre, Pertussis epidemiology in Australia over the decade 1995–2005—trends by region and age group. Commun Dis Intell 31, 205–215 (2007).
D.W. Jackson, P. Rohani, Perplexities of pertussis: Recent global epidemiological trends and their potential causes. Epidemiol Infect (2013).
L.P. Celentano i in., Resurgence of pertussis in Europe. Pediatr Infect Dis J 24, 761–765 (2005).
10. J.D. Cherry, Epidemic pertussis in 2012—the resurgence of a vaccine-preventable disease. N Engl J Med 367, 785–787 (2012).
T.A. Clark, N.E. Messonnier, S.C. Hadler, Pertussis control: Time for something new? Trends Microbiol 20, 211–213 (2012).
L. Zhang, S.O. Prietsch, I. Axelsson, S.A. Halperin, Acellular vaccines for preventing whooping cough in children. Cochrane Database Syst Rev 3, CD001478 (2012).
R. Higgs i in., Immunity to the respiratory pathogen Bordetella pertussis. Mucosal Immunol 5, 485–500 (2012).
M.J. Friedrich, Research aims to boost pertussis control. JAMA 306, 27–29 (2011).
G.A. Poland, Pertussis outbreaks and pertussis vaccines: New insights, new concerns, new recommendations? Vaccine 30, 6957–6959 (2012).
S. Elahi, J. Holmstrom, V. Gerdts, The benefits of using diverse animal models for studying pertussis. Trends Microbiol 15, 462–468 (2007).
J.M. Warfel, J. Beren, V.K. Kelly, G. Lee, T.J. Merkel, Nonhuman primate model of pertussis. Infect Immun 80, 1530–1536 (2012).
J.M. Warfel, J. Beren, T.J. Merkel, Airborne transmission of Bordetella pertussis. J Infect Dis 206, 902–906 (2012).
M.A. Witt i in., Reduced risk of pertussis among persons ever vaccinated with whole cell pertussis vaccine compared to recipients of acellular pertussis vaccines in a large US cohort. Clin Infect Dis 56, 1248–1254 (2013).
20. J. Liko, S.G. Robison, P.R. Cieslak, Priming with whole-cell versus acellular pertussis vaccine. N Engl J Med 368, 581–582 (2013).
S.L. Sheridan i in., Number and order of whole cell pertussis vaccines in infancy and disease protection. JAMA 308, 454–456 (2012).
N.P. Klein i in., Comparative effectiveness of acellular versus whole-cell pertussis vaccines in teenagers. Pediatrics 131, e1716–1722 (2013).
H.E. Rowlands i in., Impact of rapid leukodepletion on the outcome of severe clinical pertussis in young infants. Pediatrics 126, e816–e827 (2010).
J.K. Kolls, S.A. Khader, The role of Th17 cytokines in primary mucosal immunity. Cytokine Growth Factor Rev 21, 443–448 (2010).
S. Wei i in., Th17 cells have stem cell-like features and promote long-term immunity. OncoImmunology 1, 516–519 (2012).
C.J. Pitcher i in., Development and homeostasis of T cell memory in rhesus macaque. J Immunol 168, 29–43 (2002).
R. Libster, K.M. Edwards, Re-emergence of pertussis: What are the solutions? Expert Rev Vaccines 11, 1331–1346 (2012).
D. Greco i in., A controlled trial of two acellular vaccines and one whole-cell vaccine against pertussis. N Engl J Med 334, 341–348 (1996).
L. Gustafsson i in., A controlled trial of a two-component acellular, a five-component acellular, and a whole-cell pertussis vaccine. N Engl J Med 334, 349–355 (1996).
30. L.K. Misegades i in., Association of childhood pertussis with receipt of 5 doses of pertussis vaccine by time since last vaccine dose, California, 2010. JAMA 308, 2126–2132 (2012).
N.P. Klein i in., Waning protection after fifth dose of acellular pertussis vaccine in children. N Engl J Med 367, 1012–1019 (2012).
S.Y. Tartof i in., Waning immunity to pertussis following 5 doses of DTaP. Pediatrics 131, e1047–e1052 (2013).
M.A. Witt, P.H. Katz, D.J. Witt, Unexpectedly limited durability of immunity following acellular pertussis vaccination in preadolescents in a North American outbreak. Clin Infect Dis 54, 1730–1735 (2012).
J.L. Deen i in., Household contact study of Bordetella pertussis infections. Clin Infect Dis 21, 1211–1219 (1995).
U. Heininger, W.J. Kleemann, J.D. Cherry, A controlled study of the relationship between Bordetella pertussis infections and sudden unexpected deaths among German infants. Pediatrics 114, e9–e15 (2004).
J.M. Warfel, T.J. Merkel, Bordetella pertussis infection induces a mucosal IL-17 response and long-lived Th17 and Th1 immune memory cells in nonhuman primates. Mucosal Immunol 6, 787–796 (2013).
C. Andreasen, D.A. Powell, N.H. Carbonetti, Pertussis toxin stimulates IL-17 production in response to Bordetella pertussis infection in mice. PLoS ONE 4, e7079 (2009).
X. Zhang i in., Interleukin-1 receptor signaling is required to overcome the effects of pertussis toxin and for efficient infection- or vaccination-induced immunity against Bordetella pertussis. Infect Immun 79, 527–541 (2011).
N.K. Fennelly i in., Bordetella pertussis expresses a functional type III secretion system that subverts protective innate and adaptive immune responses. Infect Immun 76, 1257–1266 (2008).
40. X. Zhang i in., Decreased leukocyte accumulation and delayed Bordetella pertussis clearance in IL-6-/- mice. J Immunol 186, 4895–4904 (2011).
S.C. Higgins i in., TLR4 mediates vaccine-induced protective cellular immunity to Bordetella pertussis: Role of IL-17-producing T cells. J Immunol 177, 7980–7989 (2006).
P.J. Ross i in., Relative contribution of Th1 and Th17 cells in adaptive immunity to Bordetella pertussis. PLoS Pathog 9, e1003264 (2013).
R.M. Schure i in., T-cell responses before and after the fifth consecutive acellular pertussis vaccination in 4-year-old Dutch children. Clin Vaccine Immunol 19, 1879–1886 (2012).
R.M. Schure i in., Pertussis circulation has increased T-cell immunity during childhood more than a second acellular booster vaccination in Dutch children 9 years of age. PLoS ONE 7, e41928 (2012).
C.H. Sørensen, P.L. Larsen, IgD in nasopharyngeal secretions and tonsils from otitis-prone children. Clin Exp Immunol 73, 149–154 (1988).
O. Pabst, New concepts in the generation and functions of IgA. Nat Rev Immunol 12, 821–832 (2012).
D.L. Perry, L. Bollinger, G.L. White, The Baboon (Papio spp.) as a model of human Ebola virus infection. Viruses 4, 2400–2416 (2012).
K. Schroder, P.J. Hertzog, T. Ravasi, D.A. Hume, Interferon-gamma: An overview of signals, mechanisms and functions. J Leukoc Biol 75, 163–189 (2004).
C.M. Ausiello i in., Vaccine- and antigen-dependent type 1 and type 2 cytokine induction after primary vaccination of infants. Infect Immun 65, 2168–2174 (1997).
50. F.Y. Lai i in., Comparative seroepidemiology of pertussis, diphtheria and poliovirus antibodies in Singapore. Vaccine 30, 3566–3571 (2012).
51. L.A. Castagnini i in., Impact of maternal postpartum tetanus and diphtheria toxoids and acellular pertussis immunization on infant pertussis infection. Clin Infect Dis 54, 78–84 (2012).
52. L. Nilsson i in., Pertussis vaccination in infancy lowers the incidence of pertussis disease and the rate of hospitalisation. Vaccine 30, 3239–3247 (2012).
53. Committee on Care and Use of Laboratory Animals, Guide for the Care and Use of Laboratory Animals. NIH (1985).
54. B.D. Meade i in., Description and evaluation of serologic assays used in a multicenter trial of acellular pertussis vaccines. Pediatrics 96, 570–575 (1995).