W USA rejestruje się mniej niż 1% NOPów – Harvard Pilgrim Health Care
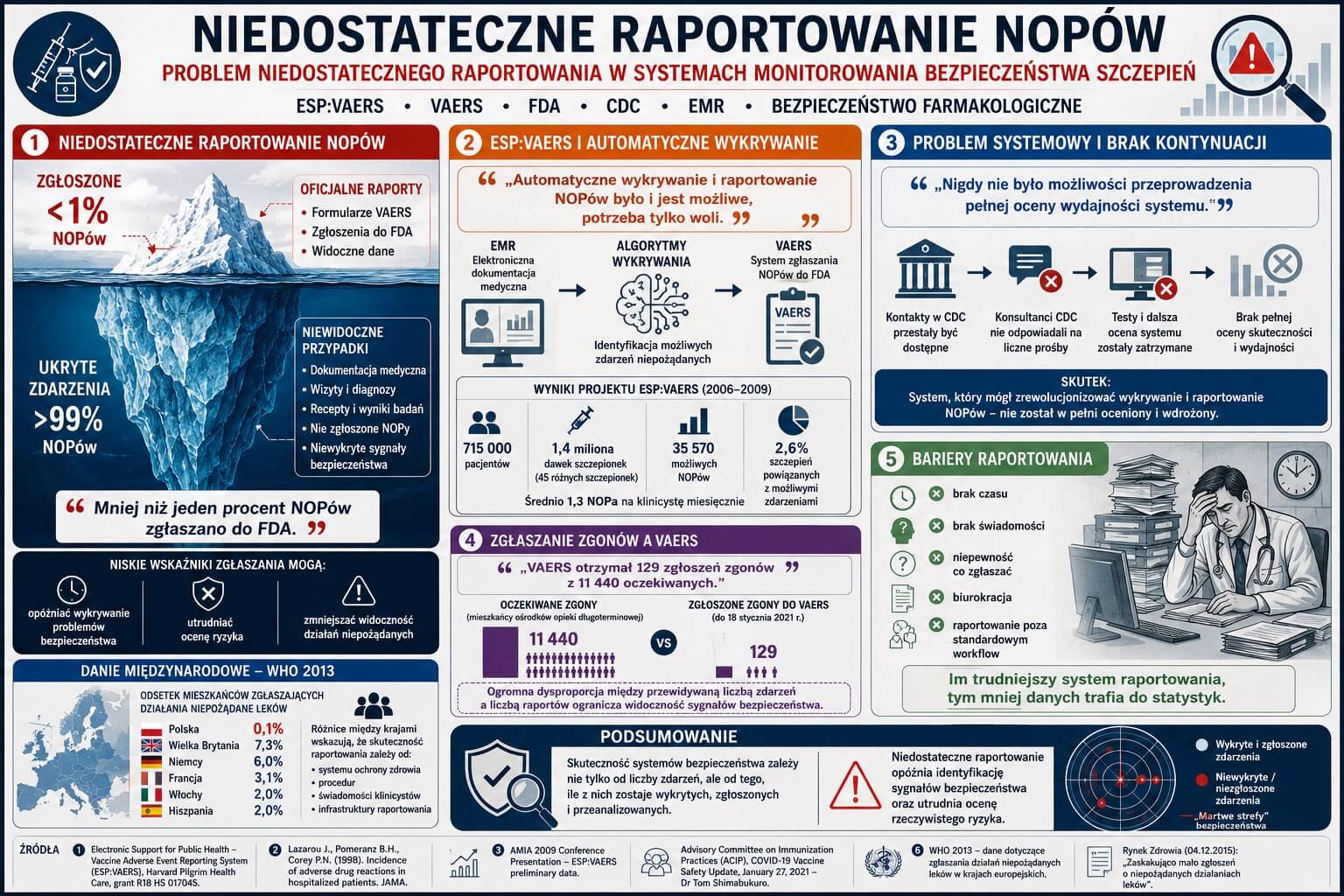
Podsumowanie projektu Electronic Support for Public Health – Vaccine Adverse Event Reporting System (ESP:VAERS) (Massachusetts)
Działania niepożądane związane ze szczepionkami są częste, ale niedostatecznie raportowane, przy czym mniej niż jeden procent [NOPów] zgłaszany jest do Agencji ds. Żywności i Leków (FDA). Niskie wskaźniki zgłaszania uniemożliwiają lub opóźniają identyfikację „problematycznych” szczepionek, potencjalnie zagrażając zdrowiu społeczeństwa. Potrzebne są nowe metody nadzoru nad działaniami niepożądanymi leków i szczepionek. Proaktywne, spontaniczne, zautomatyzowane zgłaszanie zdarzeń niepożądanych wbudowane w elektroniczną dokumentację medyczną (EMR – electronic medical record) i inne systemy informacyjne mogą potencjalnie przyspieszyć identyfikację problemów związanych z nowymi szczepionkami i dokładniej oszacować ryzyko starszych.
Projekt „Elektroniczne Wsparcie Zdrowia Publicznego: System Zgłaszania Niepożądanych Odczynów Poszczepiennych [Electronic Support for Public Health – Vaccine Adverse Event Reporting System – ESP: VAERS] miał na celu stworzenie uogólnionego systemu ułatwiającego wykrywanie i zgłaszanie przez klinicystę niepożądanych odczynów poszczepiennych [NOP]. Zastosowano elektroniczną dokumentację medyczną [EMR] dostępną ze wszystkich wizyt ambulatoryjnych w dużej wielospecjalistycznej placówce. Każdy pacjent otrzymujący szczepionkę był automatycznie identyfikowany i przez kolejne 30 dni, ich kody diagnostyczne, testy laboratoryjne i recepty na leki były oceniane pod kątem wartości sugerujących zdarzenie niepożądane.
System monitorowania bezpieczeństwa szczepionek ledwo zipie, w czasie gdy miliony ludzi się szczepi w USA.
Anafilaksja po szczepieniu, VAERS wyłapuje w okolicach 1%
Głównymi celami tego projektu były:
1. Zidentyfikowanie wymaganych elementów danych i opracowanie systemów do monitorowania elektronicznej dokumentacji medycznej w opiece ambulatoryjnej pod kątem zdarzeń niepożądanych po podaniu szczepionki.
2. Przygotowanie i bezpieczne przesyłanie elektronicznych raportów zatwierdzonych przez klinicystę/lekarza do krajowego Systemu Zgłaszania Niepożądanych Odczynów Poszczepiennych VAERS.
3. Kompleksowa ocena działania ESP: VAERS [Elektronicznego Wsparcia Zdrowia Publicznego: System Zgłaszania Niepożądanych Odczynów Poszczepiennych] i wydajności w randomizowanym badaniu i porównanie tego projektu z istniejącymi bazami danych VAERS i Vaccine Safety Datalink [VSD].
4. Dystrybucja dokumentacji i oprogramowania opracowanego oraz udoskonalonego, które są przenośne, do innych placówek opieki ambulatoryjnej, a także do innych systemów elektronicznej dokumentacji medycznej.
Wstępne dane zbierano od czerwca 2006 roku do października 2009 roku od 715.000 pacjentów. Łącznie 1.4 miliona dawek szczepionek (spośród 45 różnych szczepionek) podano 376.452 osobom. Z tej ilości podanych dawek zidentyfikowano 35.570 możliwych reakcji poszczepiennych (2,6 procent szczepień). Jest to średnio 1,3 niepożądanego odczynu poszczepiennego na klinicystę miesięcznie. Zespół doszedł do wniosku, że możliwym jest automatyczne wykrywanie niepożądanych odczynów poszczepiennych [NOPów] w tak określony sposób i elektroniczne zgłaszanie ich do bazy VAERS. Funkcje wspomagania decyzji mogą zostać zmienione, aby oprócz wykrywania chorób podlegających zgłaszaniu można było wykrywać zdarzenia związane ze szczepieniem, jako potencjalne niepożądane odczyny poszczepienne.
Fragment raportu końcowego dla grantu R18 HS 017045
Wstępne dane zbierano od czerwca 2006 r. do października 2009 r. na od 715.000 pacjentów. Podano 1,4 miliona dawek (spośród 45 różnych szczepionek) 376.452 osobom. Z tej ilości podanych dawek zidentyfikowano 35.570 możliwych niepożądanych odczynów poszczepiennych (2,6 procent szczepień). Jest to średnio 890 możliwych niepożądanych odczynów poszczepiennych, średnio 1,3 NOPa na lekarza, na miesiąc. Dane te zostały zaprezentowane na konferencji AMIA w 2009 roku.
Ponadto badacze w projekcie ESP: VAERS wzięli udział w panelu, aby zbadać perspektywy klinicystów, sprzedawców elektronicznej dokumentacji medycznej (EHR), przemysłu farmaceutycznego i FDA w kierunku systemów wykorzystujących proaktywne, zautomatyzowane systemy zgłaszania zdarzeń niepożądanych.
W USA rejestruje się mniej niż 1% NOPów
Zdarzenia niepożądane związane ze stosowaniem leków i szczepionek są częste, ale niedostatecznie zgłaszane i wpisywane do statystyk. Chociaż 25% pacjentów leczonych ambulatoryjnie doświadczyło negatywnych skutków ubocznych, to mniej niż 0,3% wszystkich zdarzeń niepożądanych i 1-13% poważnych efektów ubocznych zgłaszane jest do Agencji ds. Żywności i Leków (FDA). Podobnie jest w przypadku szczepionek, zgłaszano mniej niż 1% niepożądanych odczynów poszczepiennych [NOPów]. Niskie wskaźniki zgłaszania uniemożliwiają lub spowalniają identyfikację „problematycznych” leków i szczepionek zagrażających zdrowiu publicznemu. Potrzebne są nowe metody nadzoru pod kątem działań niepożądanych leków i szczepionek. Bariery w raportowaniu obejmują brak świadomości klinicysty, niepewność co do tego, kiedy i co zgłaszać, a także obciążenia związane ze zgłaszaniem: zgłaszanie [efektów ubocznych] nie jest częścią zwykłego toku pracy klinicystów, wymaga czasu i jest powielane. Proaktywne, spontaniczne, zautomatyzowane zgłaszanie zdarzeń niepożądanych wbudowane w elektroniczną dokumentację medyczną i inne systemy informacyjne może potencjalnie przyspieszyć identyfikację problemów z nowymi lekami i bardziej ostrożną ilościową ocenę ryzyka starszych leków.
Niestety, nigdy nie było możliwości przeprowadzenia oceny wydajności systemu, ponieważ niezbędne kontakty w Centrum Kontroli i Prewencji Chorób [CDC] przestały być już dostępne, a konsultanci CDC odpowiedzialni za otrzymywanie danych nie reagowali już na nasze liczne prośby o kontynuowanie testów i oceny.
Zobacz na: Czy na pewno szczepionki to najlepiej przebadane produkty firm farmaceutycznych?
Szczepionka Heplisav B firmy Dynavax – adiuwant 1018 i zawały serca
Szokujące wyniki badań szczepionki MMR. Powoduje chorobę górnych dróg oddechowych i przewodu pokarmowego – Del Bigtree [1978]
Porównanie bezpieczeństwa szczepionek MMR – MMR-RIT (Priorix) firmy GSK z MMR 2 firmy Merck – Del Bigtree
„Według Światowej Organizacji Zdrowia (WHO), w 2013 r. w Polsce działania niepożądane leków zgłosiło jedynie 0,1 proc. mieszkańców, podczas gdy w Wielkiej Brytanii 7,3 proc., Niemczech 6 proc., we Francji 3,1 proc. oraz we Włoszech i Hiszpanii – po 2 proc.” – Źródło: Rynek Zdrowia, Zaskakująco mało zgłoszeń o niepożądanych działaniach leków, 04.12.2015 http://www.rynekzdrowia.pl/Farmacja/Eksperci-zaskakujaco-malo-zgloszen-o-niepozadanych-dzialaniach-lekow,157349,6.html
Zgłaszanie zgonów jako NOPy po eksperymentalnych szczepionkach na C-19
Po uruchomieniu akcji eksperymentalnych szczepień „ludzkich królików doświadczalnych”, urzędnicy ds. zdrowia publicznego w USA, spodziewając się, że może dojść do zgonów staruszków, gdy zaczną ich szczepić, postanowili opracować dla siebie dupochron.
27 stycznia 2021 roku Komitet Doradczy ds. Praktyk Szczepień (ACIP) opublikował dokument dotyczący bezpieczeństwa szczepionek na Covid-19.
Jedną z podanych informacji w tym dokumencie na str. 36 jest ustalenie bazowej liczby zgonów rezydentów domów opieki. Aby móc mówić, że szczepionki przyczyniają się do zwiększonej liczby zgonów to ilość raportowanych zgonów musiałaby przekroczyć liczbę bazową. Niepożądany Odczyn Poszczepienny to każde pogorszenie stanu zdrowia w okresie 4 tygodni po podaniu szczepionki.
Mimo iż wydano nakaz raportowania komplikacji po szczepieniach ich ustalenia przypadkowo przekazują wskazówkę dotyczącą raportowania zgonów poszczepiennych. Mianowicie ilość raportowanych zgonów do Systemu Zgłaszania Niepożądanych Odczynów Poszczepiennych VAERS wynosi około 1.1%.
Szacowana umieralność w ośrodkach opieki długoterminowej
— Wśród 1,3 miliona mieszkańców ośrodków opieki długoterminowej (2M x 65%) zaszczepionych w 29-dniowym okresie ryzyka (21 grudnia – 18 stycznia)
– Spodziewamy się 11.440 zgonów wśród mieszkańców ośrodków opieki długoterminowej (= 286.000*4%) po szczepieniu.
— Dla porównania, system raportowania NOPów VAERS otrzymał 129 zgłoszeń o zgonach po szczepieniu COVID-19 u mieszkańców ośrodków opieki długoterminowej do 18 stycznia 2021 roku.
— Śmiertelność wśród pensjonariuszy ośrodków opieki długoterminowej jest wysoka i znaczna liczba zgonów w tej populacji wystąpi po zaszczepieniu jako czasowo powiązane przypadkowe zdarzenia.” – COVID-19 vaccine safety update. Advisory Committee on Immunization Practices (ACIP) January 27, 2021. Dr Tom Shimabukuro
„Wszystkie raporty VAERS są traktowane jako poufne zgodnie z wymogami prawa. Do udostępnienia VAERS dokumentacji medycznej nie jest wymagana zgoda pacjenta. W 2012 roku zgłoszenia otrzymano od świadczeniodawców opieki zdrowotnej (41%), producentów (29%), innych źródeł (17%) oraz osób lub rodzin szczepionych (14%).” – AAP, Vaccine Adverse Event Reporting System plays vital role in safety :

https://szczepienia.pzh.gov.pl/faq/jak-wygladaja-badania-kliniczne-iv-fazy-po-dopuszczeniu-szczepionki-do-obrotu/
– Badania kliniczne IV fazy nazywane są inaczej badaniami porejestracyjnymi.
– Prowadzone są przez cały czas obecności szczepionki na rynku.
– Wszystkie szczepionki stosowane w Programie Szczepień Ochronnych objęte są badaniami IV fazy.
Badania kliniczne IV fazy obejmuje szeroki panel badań prowadzonych kiedy szczepionka została dopuszczona do obrotu (zarejestrowana) i jest dostępna na rynku. Stąd też IV faza badań często nazywana jest badaniami porejestracyjnymi. W czasie badań IV fazy potwierdzane jest bezpieczeństwo produktu we wszystkich wskazaniach zaakceptowanych w procesie rejestracji szczepionki. W tej fazie weryfikowane są również wyniki uzyskane w poprzednich etapach badań klinicznych. W ramach IV fazy badane są również nowe wskazania dla zarejestrowanego już produktu, w nowych szczególnych grupach, np. przewlekle chorych oraz kontynuowana jest ocena czasu utrzymywania się odporności. Monitorowane jest bezpieczeństwo szczepionek.
Badania IV fazy obejmują również badania obserwacyjne, w tym porównanie okresu sprzed wprowadzenia szczepień z okresem po ich wprowadzaniu, co pozwala ocenić jak szczepionka działa w praktyce.
Ważnym i wymaganym elementem badań IV fazy szczepionek są również badania epidemiologiczne, w tym prowadzony nadzór nad chorobami zakaźnymi, którym można zapobiegać poprzez szczepienia oraz nadzór nad niepożądanymi odczynami poszczepiennymi.
Badania IV fazy prowadzą wytwórcy oraz instytucje związane ze zdrowiem publicznym.
„Badania IV fazy pozwalają na ocenę szczepionki w odniesieniu do dużych populacji i w długim okresie.”
Czy badania IV fazy mogą być przymusowe?